CRISPR, genoma editatzeko teknika: onurak eta kezkak
2016/03/09 Etxebeste Aduriz, Egoitz - Elhuyar Zientzia Iturria: Elhuyar aldizkaria
“Nik oraindik ez dut erabiltzen, baina seguruenik aurten hasiko naiz” dio Jose Antonio Rodríguez Pérez EHUko genetikariak. Leuzemiarekin lotuta dagoen mutazio bat ikertzeko erabili nahi du Rodríguezek CRISPR teknika. Mutazio horrek zer eragin duen aztertzeko, mutazioa duten zelulak behar ditu. “Orain arte aukera bakarra zen pazienteetatik zelulak hartzea; baina hori oso zaila da. Askoz errazagoa da guk laborategian ditugun zeluletan mutazio hori sartzea”. CRISPRekin hori egin dezake.

DNA zehaztasun handiz editatzeko balio du CRISPR teknikak. DNA-zatiak kendu daitezke nahi den lekuan, eta baita zati berriekin ordezkatu ere. Hori, dena den, ez da berria, lehendik ere baziren hori egiteko beste teknika batzuk. “Garrantzitsuena da gauzak asko erraztu eta merketu egin dituela” azpimarratu du Rodríguezek.
CRISPRen oso antzeko beste tresna batzuk ere baziren, TALEN eta ZFN kasu. “Tresna horiek CRISPRek egiten duen gauza bera egiten dute; baina horiek erabiltzeko diseinatu eta muntatu behar duzu proteina bat, eta hori oso garestia da. CRISPRekin, berriz, diseinatu behar duzu RNA molekula bat, eta hori oso merkea da. Demagun 100 euro behar direla horretarako, bada aurreko teknikekin milaka euro beharko lirateke”.
Demokratizazioa
Gauzak hainbeste errazteak aukerak asko zabaltzen ditu. “Gauza desberdinak probatu ditzakezu. Proiektu asko probak egitean oinarritzen dira, eta horretarako 5.000 euro inbertitu behar badituzu, ba igual ez zara horretan hasiko, baina 200 euro badira, probatu dezakezu”, azaldu du Rodríguezek. Gainera, “demokratizatu egin ditu esperimentu hauek; lehen ezin zuen jende askok egin ahal izango ditu. Lehen halako proiektuak ezin genituen egin laborategi txikiek, baina orain CRISPRekin bai. Horregatik zabaldu da hain azkar eta modu esponentzial honetan”.
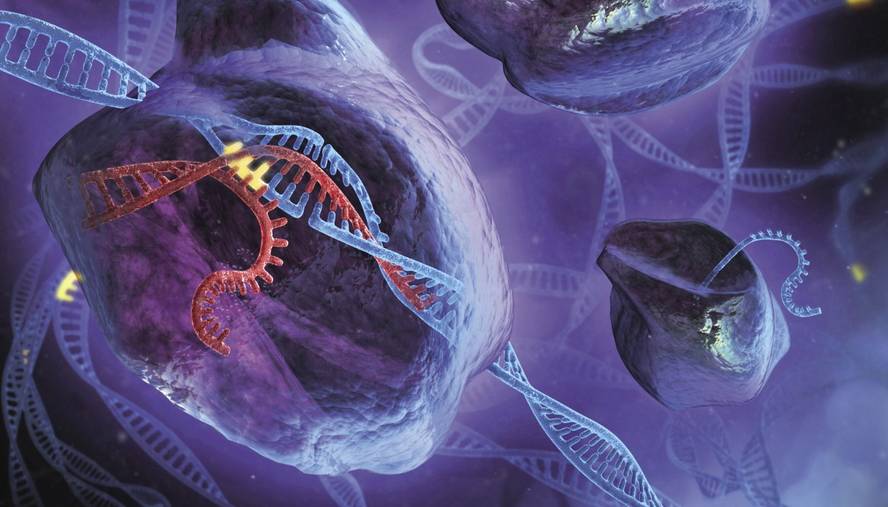
2012an argitaratu zuten Sciencen Jennifer Doudnak eta Emmanuelle Charpentierrek bakterioen CRISPR-Cas9 konplexu entzimatikoa edizio genetikorako tresna gisa erabili zitekeela. Konplexu hori RNA gida batek eta Cas9 entzimak osatzen dute. Entzimak DNA mozten du, zehazki RNA gidak esaten dion tokian. Hala, genoma nahi den lekuan editatu daiteke, leku horrekiko osagarria den RNA sintetizatuta.
Oinarrizko ikerketarako aukera izugarriak eskaintzen ditu, eta aplikazioak ere hamaika izan daitezke. Terapia genikoa da itxaropentsuenetako bat. “Pausu erraldoia eman da”, dio Ana Aguirre Escobal EHUko genetikariak. “Orain arte terapia genikoarekin, oso garestia izateaz gain, oso emaitza on gutxi lortzen ziren, teknika ez zelako ona. Orain, berriz, emaitza horiek asko hobetzea espero da”.
Ados dago Rodríguez: “Gaixotasun batzuen kasuan, oso garrantzitsua izan daiteke. Gaixotasun monogeniko askotan ondo identifikatuta dago zein den genea, eta baita zein diren akatsak, eta nola zuzendu. Baina, orain arte ezin zen gene bat zuzendu. Gene bat gaizki bazegoen, gene horren beste kopia zuzen bat sartzen zen”. Kopia hori bektore baten bidez sartzen zen, eta genoman nonbait txertatuko zen zoriz, eta itxaropena izan behar zen gene horrek bere funtzioa beteko zuela. Orain gene horri dagokion lekuan bertan sartu daiteke kopia zuzena, aurrekoa kenduta. “Orain, benetan zuzendu egin daitezke geneak”, zehaztu du Rodríguezek.
Terapiarako bidea lantzen
2014ean MITeko ikertzaile batzuek erabili zuten lehenengoz CRISPR teknika animalia helduetan gaixotasun bat sendatzeko. Saguetan erabili zuten, gizakietan tirosinemia izeneko gibeleko gaitza eragiten duen mutazioa zuzentzeko. Gaitza sendatzea lortu zuten, baina, aldi berean, lan horrek erakutsi zuen teknikak bazituela konpondu beharreko arazo batzuk ere.
Batetik, gibeleko zeluletara Cas9 entzima eta RNA gida sartzeko erabili zuten teknika, presio handiko injekzioa, ez da egokia gizakietan aplikatzeko. Eta, bestetik, 250 zeluletatik batean bakarrik lortu zuten mutazioa zuzentzea. Kasu horretan nahikoa izan zen gaitza sendatzeko, baina oso litekeena da beste gaixotasun askoren kasuan ez izatea.
Bestalde, “CRISPRek oraindik baditu efektu ez-espezifikoak —gehitu du Rodríguezek—; batzuetan RNA lotu daiteke genomaren beste parte batean. Teknika optimizatu behar da oraindik, baina hobetzeko aukera badago. Adibidez, orain arte Cas-9 entzima erabili da, baina beste batzuk ere ari dira probatzen, eta espezifikoagoak izan daitezke”.
Saguetan tirosinemia sendatzea lortu zuen MITeko taldeak berak ere dagoeneko lortu du teknika hobetzea. Otsailean argitaratu zuten saguen gibeleko zeluletara iristeko modu seguruago eta eraginkorrago bat. Birus baten bidez sartu zituzten RNA gida eta DNA-zati zuzena, eta nanopartikulen bidez Cas9 entzima kodetzen duen RNA mezulari bat. Hala 16 zelulatik batean lortu zuten zuzenketa egitea. Eta ez zuten ia efektu ez-espezifikorik atzeman.
Badira adibide gehiago ere, adibidez, abenduan hiru ikerketa-taldek aldi berean Sciencen argitaratutako artikuluetan erakutsi zuten saguetan Duchenne muskulu-distrofia gaitza hobetzea lortu zutela. Azkar doa kontua, baina gizakietan aplikatzeko oraindik denbora beharko dela uste du Rodríguezek: “Ez dut uste hurrengo urtean egiteko moduan gaudenik, baina urte batzuk barru nik uste posible izango dela aldaketak zehaztasun handiz egitea gizakietan. Gero begiratu beharko dugu hori baimentzen den, edo nola kontrolatzen den”.
Kezkak mahai gainean
Izan ere, teknikaren ahalmena zenbatekoa argi gelditzen joan den heinean, eta zein azkar hedatzen ari den ikusita, kezka etikoak ere handitu dira. “Erraztasuna da teknika honen alde positiboa, baina baita negatiboa ere, tresna honekin ‘jolastea’ erraza baita”, adierazi du Rodríguezek. “Nik batez ere alde positiboak ikusten ditut. Izan ere, teknikaren arriskuak hor daude, baina beste teknika batzuenak aspalditik dauden bezala”.
Beste batzuek, berriz, arriskuei garrantzi handiagoa ematen diete. 2015eko martxoan, CRISPR eta gainerako teknikak giza enbrioiak eraldatzeko erabiltzearen aurka azaldu zen aditu-talde bat, Nature aldizkarian argitaratutako artikulu batean. Hori laster gerta zitekeela uste zuten aditu horiek. Eta hilabete beranduago, Txinako Sun Yat-sen Unibertsitateko ikertzaileek argitaratu zuten CRISPR teknika erabiliz giza enbrioiak eraldatu zituztela. Garatzeko aukerarik ez zuten enbrioiak erabili zituzten, baina esperimentuak lehendik zeuden kezkak hauspotu zituen.
Egoera horren aurrean, kezka horiei buruz hitz egiteko batzar bat antolatu zuten Estatu Batuetako zientzia- eta medikuntza-akademiek, Londreseko Royal Societyk eta Txinako Zientzia Akademiak. Abenduan bildu ziren Washingtonen mundu osoko 500 aditu, eta behin-behineko akordio batera iritsi ziren: ikerketarako giza genoma editatzea ez debekatzea, baina bai eraldatutako enbrioiak haurdunaldietarako erabiltzea.

“Zientziaren gauza on bat da dena oso publikoa dela. Hitz egin egiten da, eta entzun egiten da, eta gertatzen ari denaren araberako erabakiak hartzen dira”, dio Aguirrek. EHUko Gai Biologiko eta Genetikoki Eraldatutako Organismoen Ikerketako Etika Batzordeko presidente ohia da Aguirre, eta orain CRISPR dela eta sortu den eztabaida ez zaio berria egin. “Gogoan dut 1970eko hamarkadan, ingeniaritza genetikoko lehen teknikak agertu zirenean, adituak Asilomarren (California) elkartu zirela. Moratoria bat ezartzea erabaki zuten. Urte batzuk itxaron behar izan zen, teknikak seguruak zirela frogatu arte. Orain, antzeko zerbait gertatu da, hitz egin dute eta adostu dute: ‘aplikazioez hitz egiten hasi baino lehen, egin ditzagun laborategian sukalde-lanak, teknika hobetu, optimizatu eta ahalik eta seguruen egiteko’”.
Eztabaida aspaldikoa da. “Orain arte urrunekoak edo oso teorikoak ikusten ziren gauza batzuk, orain gertuago eta egingarriago ikusi dira, eta horrek azken urteotan erdi-hilda zegoen eztabaida zahar bat berpiztu du”. Horrez gain, badago kezka handitzea eragin duen beste faktore bat ere, Aguirreren ustez: “batzuek ohartarazi dute genetikoki eraldatutako organismoak arautzen eta erregulatzen dituzten lege askok, idatzita dauden bezala, kanpoan uzten dutela CRISPR teknika”. Izan ere, birkonbinazioaz eta DNA arrotzaz hitz egiten da lege horietan, baina CRISPR teknikan ez dago horrelakorik. “Ez daukat zalantzarik lege horiek egokituko direla, teknika berria ere arautzeko, baina egia da une honetan hori ez dela gertatu”.
Dena den, herrialdetik herrialdera asko aldatzen da nola araututa edo erregulatuta dagoen. Japonian, Txinan eta Indian, adibidez, giza enbrioietan eraldaketa genetikoak egitea debekatzen duten arauak daude, baina ez dute legezko ondoriorik. Errusia eta Argentinako erregulazioa, berriz, oso anbiguoa da. Estatu Batuetan, debekatua dago diru publikoz finantzatzea, baina legeak ez du debekatzen aplikazio klinikoa. Eta Europan, oro har, debekatuta dago klinikan, eta mugatuta ikerketarako. Erresuma Batuan berriki eman diete Francis Crick Institutuko ikertzaileei CRISPR teknika erabiltzeko baimena, giza enbrioien garapena ikertzeko.
Beldurrak eta itxaropenak
CRISPRek eragin dituen kezkak eta beldurrak, betikoak dira. “Funtsean, animalia eta landareei dagokionean ongi aztertu behar da eraldaketa horiek egitea segurua den edo ez, sortzen diren organismoak arriskurik izan dezaketen gizakiarentzat edo ekosistementzat”, azaldu du Aguirrek. “Gizakiari dagokionean, berriz, segurtasun-kontuei beste bat gehitzen zaie, nire ustez: norbanakoari buruz dugun kontzeptua. DNA-sekuentzia aldatzeaz hitz egitean urduri jartzen gara, nolabait gure banakotasunean eragingo duela iruditzen baitzaigu”.
Dena den, praktikan eztabaida beste plano batera pasatzen dela uste du Aguirrek: “gaixotasun genetiko bat duen pertsona bat gertu badugu, eta hori sendatzeko aukera bat badago, orduan hori da inporta zaiguna. Nik uste dut aplikazio errealak dituela ikusten denean, pertsonen bizitza hobetu dezaketen aplikazioak, gizarteak hobeto ikusiko dituela teknika hauek”.
Horixe gertatu izan da aurrerapen zientifiko askorekin. “Ernalketa lagunduarekin gertatu zen. Hasieran mespretxagarria zen, baina pixkanaka gizarteak eskatu egin du, eta dagoeneko lagundutako ernalketari esker jaiotako umeak ez dira ikusten deabru gisa, hasierakoak ikusten ziren moduan”.
Nolanahi ere, gaixotasunak sendatzea baino aplikazio eztabaidagarriagoak izan ditzake eraldaketa genetikoak; esaterako, enbrioiak eraldatzea hainbat ezaugarri hobetzeko. Aguirrek, ordea, ez du kezkatzeko arrazoi handirik ikusten oraingoz, “Teknika ahalbidetu dezakeelako gertuago ikusten den arren, nire ustez oraindik utopia bat da hori, beldur teoriko bat”.
Gainera, kontrola zorrotza dela azpimarratzen du: “Genoma aldatzeko edozein teknika aplikatzeko, terapia genikorako esaterako, hainbat batzordetatik pasa behar da. Estatu espainiarrean, adibidez, batzorde nazional bat dago, oso zorrotza, eta haren baimena lortu behar da. Baina horrez gain, ospitale batean probak egin nahi badira, ospitale horretako eta autonomia-erkidegoko batzorde etikoetatik ere pasa behar da. Dagoeneko badago egitura bat, eta izatekotan, kontrol hori zorroztu egingo da hemendik aurrera, izan ere, ez dut uste hobekuntza genetikoak sostengu sozialik duenik. Beraz, ez dut uste kezkatzeko motiborik dagoenik”.
Ekosistemak eraldatzeko arriskua
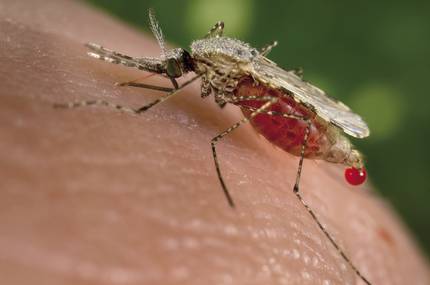
Genetikoki eraldatutako bizidunek ekosistemetan izan dezaketen eragina de beste kezketako bat. Eta kezka horiek hauspotu zituen azaroan argitaratutako beste lan batek. Malaria eragiten duen bizkarroiarekiko erresistenteak diren eltxo transgenikoak sortu zituzten Kaliforniako Unibertsitateko zientzialariek. Kasu horretan, gainera, CRISPR teknikari esker lortu zuten eraldatutako eltxo arren ondorengoen % 99k heredatzea antigorputzaren genea, eta genea aktiboa izatea eltxo horietan. Hala, kalkulatu zuten 10 belaunaldi nahikoak liratekeela gene horiek populazio batean hedatzeko.
Populazioan halako eragina izateko gaitasunak kezka handia sortu du batzuengan. Aguirrek, kasu honetan ere, dauden kontrol estuetan dauka konfiantza. “Malariaren kontrako beste eltxo transgeniko batzuk, beste teknika baten bidez eginak, askatu dira dagoeneko. Baina, horretarako 10 urteko kontrolak pasa behar izan zituzten. Horrelako baimen bat lortzeko azterketa eta ebaluazio asko eta oso sakonak egin behar dira, arriskuak eta onurak zein diren jakiteko. Egia da, horrelakoetan zero arriskurik ez dela existitzen. Kasu hartan, arrisku eta onurei buruzko txosten guztiak mahai-gainean jarri ondoren, eta malaria-maila izugarria kontuan hartuta, politikariek erabaki zuten eltxo transgenikoak askatzea. Azken finean, zientziak gizartearen eskura jartzen duen tresna bat da, eta gizarteak erabaki behar du zer egin tresna horrekin”.

Gai honi buruzko eduki gehiago
Elhuyarrek garatutako teknologia