Salsa de definición
2007/06/01 Kortabitarte Egiguren, Irati - Elhuyar Zientzia Iturria: Elhuyar aldizkaria

Pesado significa alta densidad en su uso habitual. Metal significa elemento puro o aleación de elementos metálicos. La denominación de metal pesado se ha utilizado durante años, pero suscita dudas entre los expertos. ¿Es necesario definir o clasificar metales? Es decir, ¿los elementos que entran en este saco tienen cierto carácter colectivo?
Los gases nobles, por ejemplo, son elementos del grupo 18 de la tabla periódica. Todos ellos son átomos estables y químicamente poco reactivos. Esto les confiere un cierto carácter colectivo. Los metales son elementos capaces de conducir electricidad y con brillo metálico. También pueden formar cationes y contienen óxidos básicos. Todas estas características son iguales. Sin embargo, tal vez esta definición no aclare mucho. De hecho, según esta definición, la mayoría de los elementos de la Tabla Periódica pueden ser metales. Por ello, los metales se distribuyen en grupos más pequeños en función de sus características propias y de su uso. Dentro de esta distinción se encuentran los metales pesados, nombre que se ha venido utilizando durante años entre los químicos y que se sigue utilizando en la actualidad, a pesar de las incertidumbres que plantea. La Unión Internacional para la Química Pura y Aplicada (IUPAC) aún no ha dado su definición (es un organismo normativo de referencia en el ámbito de la Química que establece, entre otras, normas para la designación de compuestos químicos). Es más, ha publicado varios informes sobre el debate sobre la definición de metales pesados.
Sin criterio
Según un informe del IUPAC, durante años se han tenido en cuenta diferentes criterios para la definición de metales pesados. Se han utilizado como criterios la densidad, la masa atómica, el número atómico y la toxicidad, entre otros. Así, en la bibliografía se recogen varias definiciones. Sin embargo, como la denominación se ha utilizado durante años sin ningún criterio concreto, existen contradicciones entre unas definiciones y otras. La denominación de metales pesados también se ha utilizado para los semi-metales, como el arsénico en algunos casos. No hay nada claro.
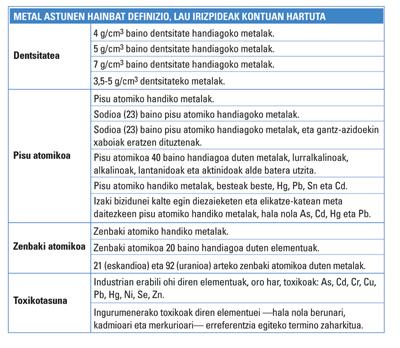
Curiosamente, la denominación de metal pesado se utilizaba hasta 1936 para designar armas grandes o grandes talentos o capacidades. En cuanto a los elementos químicos, una de las referencias más antiguas al término aparece en la tercera edición del libro Inorganic Chemistry, publicado ese mismo año en Londres. Sin embargo, esta definición no ha sido utilizada en publicaciones posteriores. La definición dada por Bjerrum tomaba como criterio la densidad de los elementos. En concreto, el metal pesado tocaba elementos de densidad superior a 7 g/cm 3. Con los años esta definición se ha ido modificando modificando el límite de densidad.
Aunque la clasificación por densidad estaba relacionada con la reactividad, algunos expertos encontraron que la densidad no tenía una importancia capital en la reactividad de los metales. Por ello, las definiciones se han adaptado a partir de la masa o peso atómico. Esto ha aproximado de alguna manera la definición a la tabla periódica. Es decir, la fuente de información más conocida sobre la clasificación de los elementos químicos. Sin embargo, no creáis que este criterio en función de la masa tampoco está nada claro.
H. Bennet y R. J. Según los editores Lewis, por ejemplo, se pueden considerar como metales pesados aquellos elementos que tienen una masa atómica mayor que el sodio (Na), es decir, mayor de 23, por lo que los que se encuentran a partir del magnesio (Mg). G. M. Por su parte, Rand y su equipo afirman que los metales pesados son elementos con una masa atómica superior a 40, es decir, a partir del escandio (Sc).

Otras definiciones se basan en el número atómico. Entre ellos, al menos unos pocos expertos o definiciones coinciden: los metales pesados son aquellos que tienen un número atómico superior a 20, es decir, los que van desde el sodio (Na). Sin embargo, existe un pequeño problema: en este grupo se incluyen el magnesio (Mg) y el potasio (K), siendo la densidad de ambos muy baja. Es decir, no se ajusta en absoluto a la definición de densidad como criterio. Ni siquiera a partir de uno de los límites más bajos de densidad.
La toxicidad es otro criterio ampliamente utilizado en la clasificación de metales pesados. Sin otra base, por su toxicidad para el medio ambiente, algunos elementos como el plomo (Pb), el cadmio (Cd) y el mercurio (Hg) se consideran metales pesados, y sus compuestos.
Sin embargo, la toxicidad de los metales pesados en general no está relacionada con sus características intrínsecas sino con su concentración. Es más, a menudo, la toxicidad depende del compuesto que lo forman. Por ejemplo, las características del estaño y del óxido de tribultilestaño son muy diferentes. La toxicidad del primero es muy baja, mientras que la segunda es bastante tóxica. Algo parecido ocurre con el cromo. El cromo no es tóxico en acero inoxidable, mientras que el ion cromato lo relaciona con el cáncer de pulmón. Este es, por tanto, el motivo por el que se descarta el concepto de metales pesados. De hecho, no tiene mucho sentido introducir metales y sus compuestos en el mismo saco de la toxicidad.
Término obsoleto

Once definiciones, muchas dudas y nada claro. Es decir, sin un claro carácter colectivo para los metales pesados. De hecho, a pesar de las características comunes de los metales, cada uno tiene sus características físico-químicas. No sólo eso, cada uno de ellos puede formar varios compuestos, cada uno de los cuales tiene sus propias características. Por tanto, no tiene mucho sentido la inclusión de metales en un mismo grupo y sus compuestos.
Por ello, según el comité de expertos del IUPAC, sería conveniente prescindir del concepto de metales pesados, ya que carece de base científica. Además, en la actualidad, como se ha mencionado anteriormente, el concepto de metales pesados se asocia a menudo con un grupo de elementos o compuestos que pueden tener relación con la contaminación y la toxicidad. Sin embargo, este grupo de expertos no hace ninguna relación directa entre la densidad y el resto de características físicas químicas (masa atómica, número atómico, etc.) y la toxicidad.

Por tanto, desde un punto de vista académico, se puede decir claramente que el concepto de metales pesados está obsoleto y debería ser descartado. Sin embargo, será difícil extender este punto de vista de la academia a la sociedad, y aun lográndolo, todavía habría un problema con la denominación de metal. De hecho, en la actualidad se utiliza el término metal para referirse tanto a los metales como a sus compuestos. Esto significa que los metales y sus compuestos son tratados como si fueran de las mismas características físico-químicas, biológicas y toxicológicas, y esto no es así.
Lo contrario ocurre en el caso del carbono. Es decir, no se utiliza la denominación de carbono para representar todos los compuestos del carbono. De hecho, si esto fuera así, el carbono sería considerado como un ser humano cancerígeno, ya que algunos de sus compuestos son cancerígenos. Por lo tanto, los metales, al igual que los compuestos carbonosos, deberían ser analizados por separado.

Gai honi buruzko eduki gehiago
Elhuyarrek garatutako teknologia