Maquinaria paira a prevención de enfermidades neurodegenerativas
2021/10/19 Lorea Velasco - Biokimikaria Iturria: Elhuyar aldizkaria
Encartado de proteínas e chapperones moleculares
As proteínas son compoñentes básicos da vida, xa que garanten o funcionamento das células. Estas moléculas, formadas por un pequeno alfabeto de vinte aminoácidos, ocúpanse como máximo das funcións que teñen lugar na célula, desde reaccións químicas até funcións estruturais. A colección de proteínas –proteoma– que hai nun organismo nun momento dado é moi variable e case infinita, aínda que toda a información paira construír a colección está codificada nos xenes.
A dogma principal da bioloxía molecular explica a transferencia de información do ADN ás proteínas, sendo o ARN mediador. A expresión dos xenes iníciase a partir da transcrición, onde, a partir da dobre molécula de ADN, prodúcese a cadea auxiliar de ARN, que será una copia desa información xenética concreta. No segundo paso, o ARN mensaxeiro volve á maquinaria denominada ribosoma, obtendo a proteína. A proteína recentemente sintetizada deberá asimilar una estrutura tridimensional adecuada paira ser funcionalmente activa, pero nas células este proceso non sempre é espontáneo.
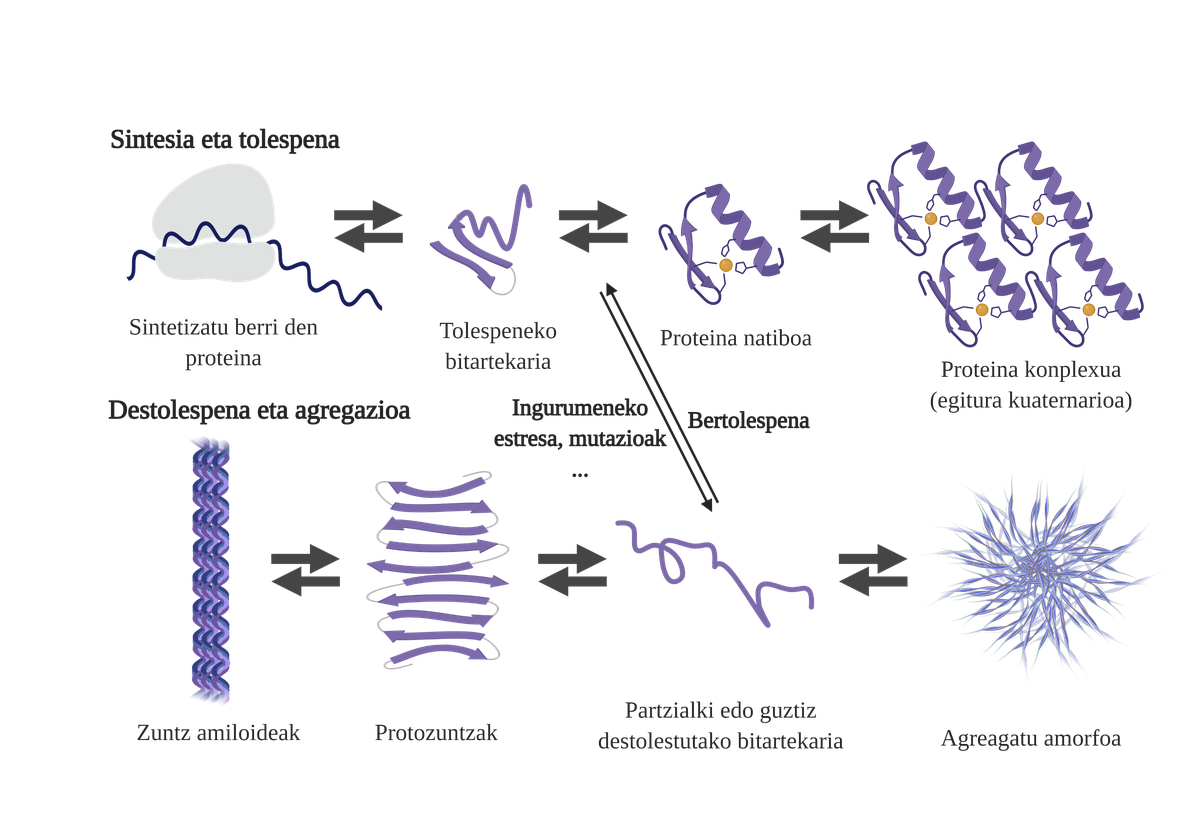
Os chaperones moleculares son esenciais nas células, xa que se encargan do control de calidade das proteínas, garantindo así a homeostasis das proteinas2. E é que moitas proteínas necesitan a axuda dos txaperones paira conseguir a súa estrutura nativ3. Sen a súa axuda poden producirse problemas no proceso de encartado da proteína e formar intermediarios mal encartados. Estes intermediarios aflorarán as zonas adhesivas que deberían estar no núcleo da proteína e tenderán á súa agregación4. Ademais, a agregación dun tipo de proteínas pode influír na agregación doutras especies de proteínas, permitindo o que se coñece como coagregación.
O proceso de encartado de proteínas recentemente sintetizadas non é a única vía paira xerar os primeiros intermediarios dos áridos. De feito, as proteínas que xa posúen una estrutura tridimensional adecuada (estrutura nativa) tamén poden sufrir destolaciones e formar intermediarios reactivos. As principais causas desta desestabilización están relacionadas con mutacións ou tensión celular, que é maior nos maiores, xa que os mecanismos de homeostasis das proteínas son máis obsoletos.
De feito, nunha situación normal, ante calquera tensión celular, os chaperones moleculares percíbeno e responden rapidamente, mantendo así a homeostasis das proteínas. Con todo, cando se van impondo ou se cronifican situacións de tensións, como as mutacións, é máis difícil garantir a calidade das proteínas das celulas6. Nestas circunstancias, a presenza de txaperones moleculares é menor paira facer fronte aos problemas de flexión das proteínas (debido á súa menor expresión ou á saturación do sistema por contrarrestar a tensión celular), aumentando a cantidade de proteínas danadas e mal plegadas7.
A agregación dificulta o funcionamento celular e provoca a aparición de enfermidades relacionadas coa flexión de proteínas como o alzheimer, o parkinson ou outras enfermidades neurodegenerativas8. De feito, varias enfermidades neurodegenerativas presentan una característica común: a acumulación de proteínas agregadas de estrutura amiloide presentes no cerebro.
Agregación e efectos dos áridos
Os procesos de agregación de proteínas nestas enfermidades son lentos e organizados. Na actualidade, o modelo máis aceptado paira explicar a formación de estruturas amiloidogénicas é a polimerización en nucleación. Segundo el, o proceso de agregación presenta una cinética característica que pode dividirse en dúas fases diferenciadas: lag ou nuclear e exponencial ou de estiramento.
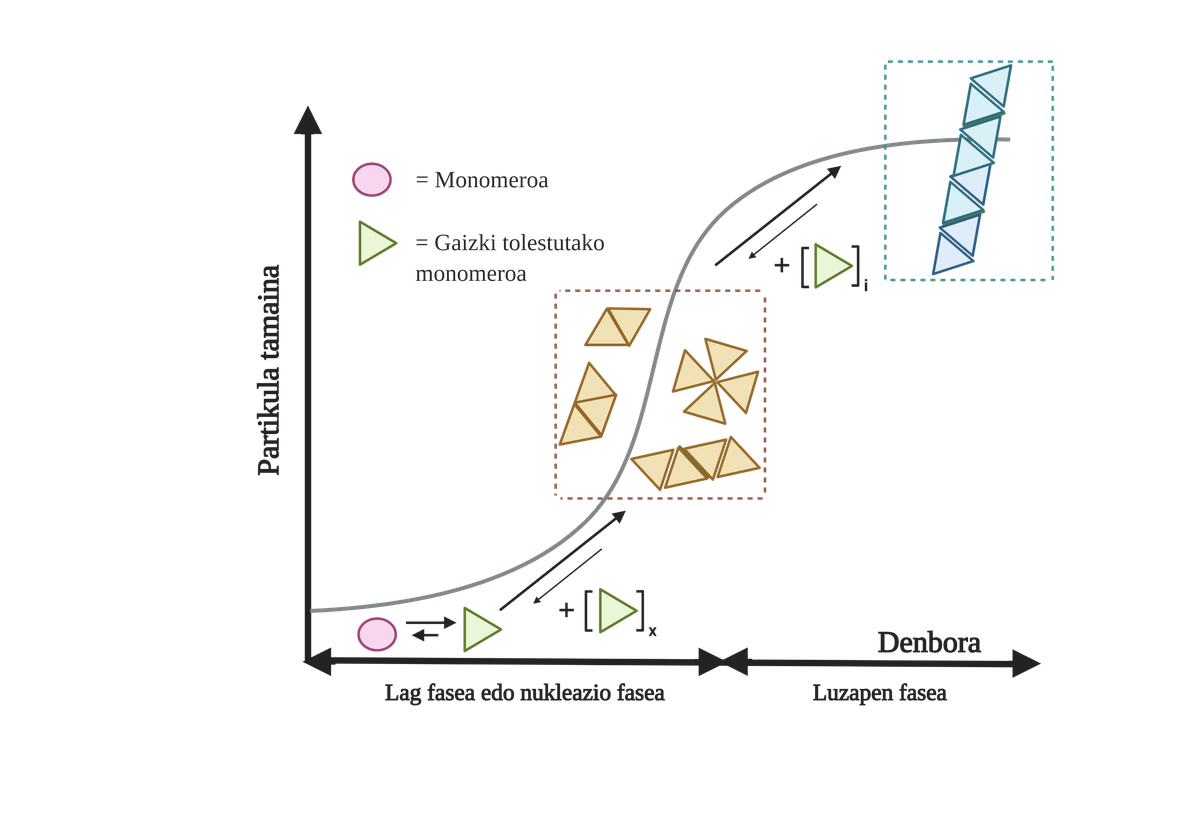
Na fase de Lag créanse os primeiros intermediarios denominados semente ou núcleo, os reactivos. Nestas estruturas fórmanse pequenos ou oligoméricos agregados de proteínas mal encartadas que se uniron entre si e que comezan a segunda fase. Estes pequenos agregados ou oligómeros acumulados en fase exponencial atraen máis proteínas formando agregados cada vez máis grandes até formar fibras amiloides 10.
Na actualidade non está do todo claro cal é o papel dos áridos, pero parece que os intermediarios da agregación son os máis tóxicos paira a célula. Segundo esta hipótese, o proceso de agregación sería, por tanto, un método de protección celular fronte a intermediarios tóxicos. En calquera caso, sábese que as acumulacións de especies amiloides son tóxicas e que a súa acumulación produce una apoptosis neuronal ou morte celular programada no cerebro.
A morte natural, precisa e programada das neuronas, a apoptosis neuronal, é un proceso imprescindible paira a maduración do sistema nervioso central. Con todo, una vez que o sistema nervioso central estea ben desenvolvido, a maioría das neuronas adultas manteranse ao longo de toda a vida do organismo, xa que a taxa de apoptosis das neuronas é moi baixa. A apoptosis precoz das neuronas ou a apoptosis aberrante mal regulada provoca a aparición de enfermidades neurodegenerativas. Tendo en conta en que zona do cerebro prodúcese a acumulación de especies amiloidogénicas e a consecuente apoptosis das neuronas, desenvolverase una enfermidade neodegenerativa diferente. Por exemplo, a perda de neuronas do hipocampo está relacionada co alzheimer, mentres que a diminución de neuronas dopaminérgicas no negro de sustancia está relacionada co parkinson 14.
O papel dos txaperones moleculares ante os intermediarios tóxicos
Ademais de contribuír ao proceso de encartado de proteínas recentemente sintetizadas, os txaperones moleculares tamén participan na replegación de intermediarios mal encartados, permitindo a desaparición de intermediarios reactivos. Por tanto, os txaperones moleculares axudan tanto na prevención como na replegación, evitando a formación de intermediarios tóxicos ou garantindo a liberación e virilización de proteínas presentes nos oligómeros cando a formación de intermediarios é inevitable.
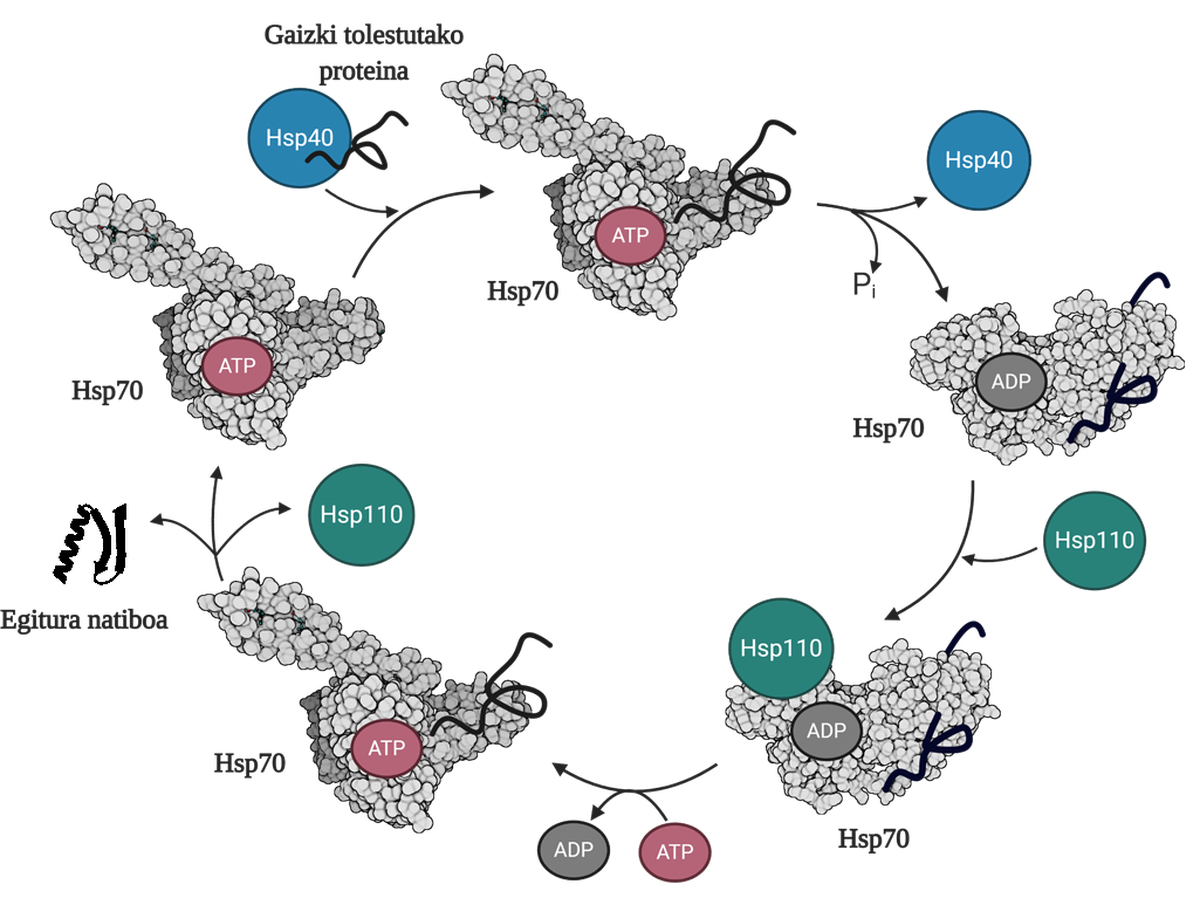
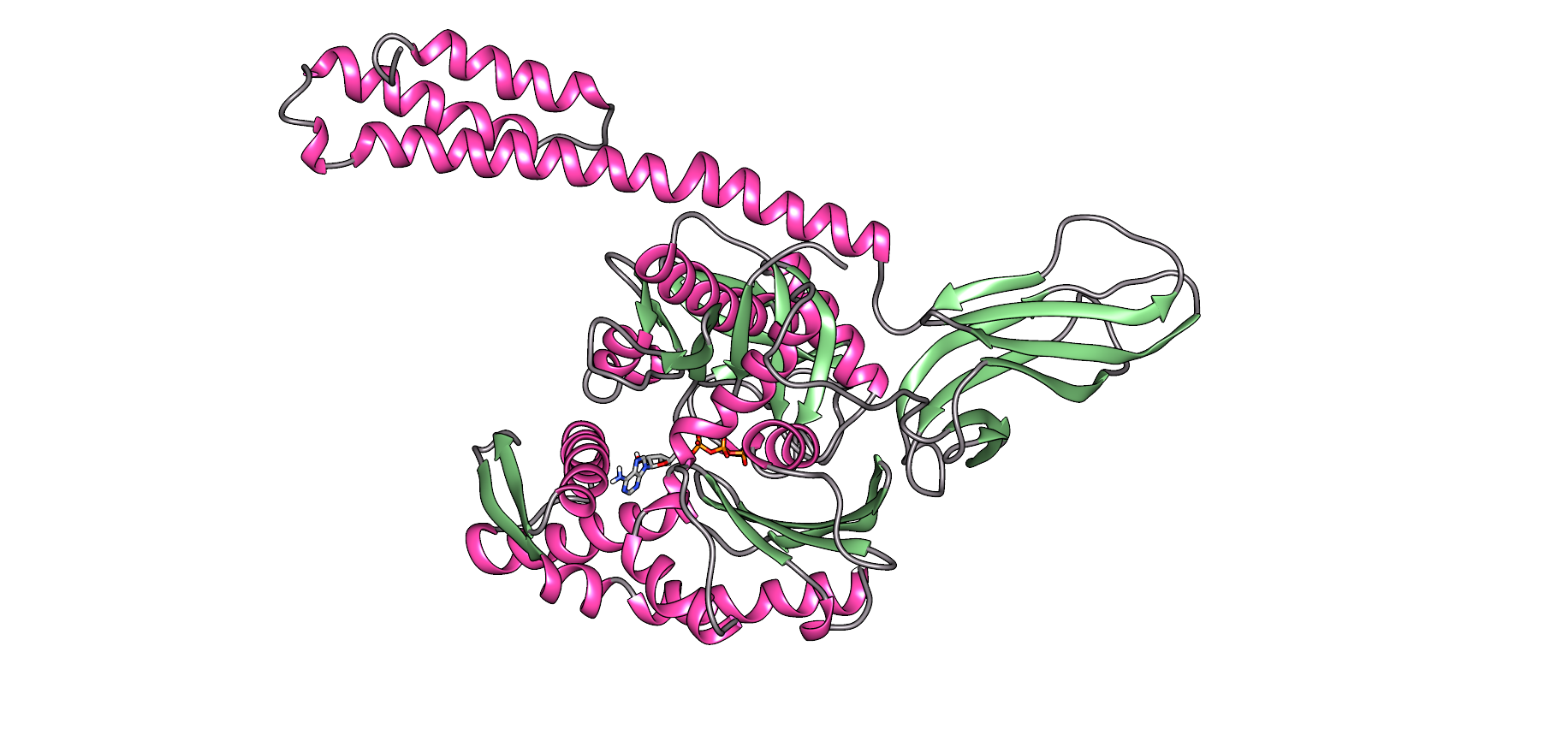
Paira permitir a rexeneración de proteínas mal encartadas ou agregadas é necesario coordinar tres familias de chapperones moleculares: Hsp70, Hsp40 e Hsp110. Entre o tres forman o sistema Hsp70, que, utilizando a enerxía mecánica liberada da hidrólisis do ATP, permite ás proteínas mal dobradas obter una estrutura nativa grazas ao proceso denominado ciclo do ATP (Figura 3). A proteína Hsp70 consta de dous dominios: o dominio de unión do nucleótido (NBD), no que teremos nucleótidos ATP ou ADP, e o dominio de unión do substrato (SBD), que dependendo do nucleótido asociado ao NBD, estará en conformado aberto ou pechado.
A proteína Hsp40 afectará a un mediador mal encartado e transferirá ao chaperón Hsp70 que está unido ao ATP, cuxo dominio SBD estará en conformación aberta en presenza do ATP. Por estimulación do substrato e da proteína Hsp40, o Hsp70 hidrólisis do ATP, quedando o ADP suxeito ao Hsp70. Nesta situación, o Hsp40a liberarase do complexo e o substrato quedará atrapado no SBD do Hsp70, xa que en presenza do ADP este dominio adquirirá una conformación pechada. Nese momento, o ciclo incluirá o Hsp110 ou o intercambiador de nucleótidos (NEF) e intercambiará o ADP que contén o Hsp70 cun novo ATP. Debido á presenza do ATP, o SBD volverá pasar ao conformado aberto e liberará o substrato ao medio. Desta forma, o substrato terá outra posibilidade de encartarse ben, normalmente será capaz de obter una estrutura nativa e a proteína Hsp70 será reciclada paira un próximo ciclo 10.
A función de desagregación/replegado do sistema Hsp70 é, por tanto, imprescindible paira evitar a acumulación de intermediarios tóxicos, xa que ademais de evitar a xeración destes tóxicos, é capaz de levar a cabo a desagregación de oligómeros xa constituídos. O funcionamento eficiente deste sistema leva a capacidade de previr enfermidades relacionadas con problemas de plegamiento como o parkinson, o alzheimer ou a esclerose lateral amiotrófica.
Cancro e apoptosis
Una das principais características do cancro é a inmortalidade das células cancerosas. A rápida división das células cancerosas e a resistencia á apoptosis son os principais responsables do aumento do tumor. As células cancerígenas utilizan diferentes vías paira evitar a apoptosis, principalmente inhibición de sinálelas prol-apoptóticas e aumento dos estímulos anti-apoptóticos. Desta forma conseguen manter as células tumorales, a pesar de sufrir unha elevada tensión, sen entrar na apoptosis. Sendo o sistema Hsp70 un mecanismo anti-tensión, nas células cancerígenas é moi frecuente a sobreexpresión do chaperón Hsp70, o que favorece a resistencia á apoptosión16.
O sistema Hsp70 como diana terapéutica ao cancro
Dada a importancia que ten o Hsp70 nas células tumorales, parece que pode ser una diana terapéutica adecuada paira reducir a resistencia das células cancerígenas aos fármacos e por tanto diminuír os tumores 17. Hai estudos que demostran que a diminución da expresión do Hsp70 é tóxica nas células cancerígenas, pero non é evidente nas células non modificadas18. A inhibición do Hsp70 afecta máis ás células tumorales, que terán prioridade de morte respecto das células normais. De feito, o fenotipo (constantemente tenso) da célula tumoral depende da función protectora do Hsp70 paira combater a citotoxicidad e por tanto evitar a apopto19. Hrrn ampliou notablemente o campo de investigación do sistema Hsp70; o uso do chaperón Hsp70 como diana ten un gran futuro, xa que pode ser útil non só paira o tratamento de enfermidades neurodegenerativas, senón tamén paira tratamentos de cancro.
Referencias
1- Crick F. 1970. “Central Dogma of Molecular Biology.” Nature, 227(5258): 561–63.
2- Fin B, Weissman, J. e Horwich, A. 2006. “Molecular Chaperones and Protein Quality Control.” Cell, 125(3): 443–51.
3- Gao X, Carroni M. Nussbaum-Krammer C, Mogk A., Nillegoda N.B., Szlachcic A. Guilbride D.L. H.R. Saibil, Mayer M.P. e B. Final. 2015 “Human Hsp70 Disaggregase Reverses Parkinson’s-Linked ?-Synuclein Amyloid Fibrils.” Molecular Cell, 59(5): 781–93.
4- Ou.T.E. 1996. “Molecular Chaperones in Cellular Protein Folding.” Nature, 381(6583): 571–79.
5- Morimoto R.I. 2008. “Proteotoxic stress and inducible chaperone networks in neurodegenerative disease and aging.” Xenes & Developement, 22(11): 1427–1438.
6- Radwan M., Wood R.J. Sui X, e Hatters D.M. 2017 “When proteostasis goes bad: protein aggregation in the cell.” IUBMB Life, 69, 49–54.7
7- Stroo E., Koopman M., Ou.A.F. Nollen e Mata-Cabana A. 2017 “Cellular Regulation of Amyloid Formation in Aging and Disease.” Forntiers in Neuroscience, 11: 64.
8- Stetler R.A., E., Zhang W., C. Ou. Liou, E. Gao, Cao G. e Chen J. 2010 “Heat Shock Proteins: Cellular and Molecular Mechanisms in the Central Nervous System.” Progress in Neurobiology, 92(2): 184–211.
9- GoM. e Spillantini M.G. 2006. “A century of Alzheimer’s disease.” Science, 314, 777–781.
10- Chaari A. 2019. “Molecular chaperones biochemistry and role in neurodegenerative diseases.” International Journal of Biological Macromolecules, 131:396-411.
11- Hartl F.U., e Hayer-Hartl M. 2009. “Converging concepts of protein folding in vitro and in vivo.” Nature Structural and Molecular Biology, 16, 574–581.
12- Awasthi A., Matsunaga E e Yamada T. 2005 “Amyloid-beta causes apoptosis of neuronal cells via caspase cascade, which can be prevented by amyloid-beta-derived short peptides.” Experimental Neurology, 196(2): 282-289.
13- Okouchi M, Ekshyyan Ou., Maracine M. e Aw T.E. 2007 “Neuronal Apoptosis in Neurodegeneration.” Antioxidants & Redox Signaling, 9(8): 1059-1096.
14- Chi H., Chang H.E e Sang T.K. 2018. “Neuronal Cell Death Mechanisms in Major Neurodegenerative Diseases.” International Journal of Molecular Sciences, 19(10): 3082.
15- Hanahan D. e Weinberg R.A. 2000. “The Hallmarks of Cancer.” Cell, 100(1): 57-70.
16- D. Brusa, C. Migliore, Garetto S., Simone M. e Matera L. 2009. “Inmunogenicity of 56 degrees C and uvc-treated prostate cancer is associated with release of HSP70 and HMGB1 from necrotic cells.” Prostate, 69: 1343–1352.
17- S. Gurbuxani, Bruey J.M. Fromentin A., C. Larmonier, Parcellier A., Jaattel M., Martín F., Solary E. e Garrido C. 2001. “Selective depletion of inducible HSP70 enhances inmunogenicity of rat colon cancer cells.” Oncogene, 20: 7478–7485.
18- Garrido C., Schmitt E., Cande C., Vahsen N., Parcellier A. e Kroemer G. 2003. “HSP27 and HSP70: potentially oncogenic apoptosis inhibitors.” Cell Cycle, 2: 579–584.
19- Kumar S., J. Strokes, Singh Ou.P., S.G. Gunn, Acharya A., Manne U. e Mishra M. 2016 “Target Hsp70: A possible therapy for cancer.” Cancer Letters, 374(1): 156-166.

Gai honi buruzko eduki gehiago
Elhuyarrek garatutako teknologia