Do laboratorio á clínica
2011/12/01 Galarraga Aiestaran, Ana - Elhuyar Zientzia Iturria: Elhuyar aldizkaria
Da mesa de traballo á cabeceira da cama (from bench to bedside), así se coñece á investigación dirixida directamente á terapia, que se está levando a cabo en diversos laboratorios que investigan no tratamento do cancro en todo o mundo. José Antonio Rodriguez traballou nun destes laboratorios até hai catro anos e, na súa opinión, "é un concepto moi interesante".
José Antonio Rodríguez é agora profesor do Departamento de Xenética da UPV. Pasou tres anos antes en Australia e outro sete en Holanda na investigación do cancro: "En Holanda traballei nun hospital, non na universidade. Traballaba no departamento de Oncoloxía Médica e alí teñen dúas liñas: nunha delas tratan aos pacientes e na outra estudan os mecanismos dos medicamentos en células tumorales que se manteñen nos preparados de crecemento. Eu traballei nesa segunda, porque son biólogo, non médico, pero as dúas liñas están estreitamente relacionadas".
Segundo Rodríguez, esta forma de traballar é apropiada paira terapias biolóxicas. "Na quimioterapia, por exemplo, os investigadores tratan de saber cal é a dose máxima que poden dar e logo dan aos pacientes una dose inferior. As terapias biolóxicas, pola súa banda, son menos tóxicas e nelas moitas veces non hai doses máximas. A súa eficacia debe ser probada doutra maneira. Trátase de medir marcadores biolóxicos (por exemplo, a concentración dunha proteína) e ver si o medicamento interfere coa sinalización celular que queremos impedir".
O bloqueo destes carreiros é a base sobre a que se asintan moitas das terapias que se están probando: a identificación dos mecanismos ou carreiros necesarios paira o crecemento, reprodución e difusión das células tumorales e a súa obstrución mediante moléculas desenvolvidas no laboratorio. Segundo explica Rodríguez, estes carreiros tamén son utilizados por células convencionais, pero non utilizan una soa, senón catro ou cinco, paira facer o mesmo. Pola contra, as células tumorales teñen una sobreactivación nunha delas e outras non as utilizan porque non as necesitan. "Esta senda de sobreactivación achega vantaxe á célula pero tamén un punto débil ao mesmo tempo ( Talón de Aquiles ). Se bloqueamos este carreiro que lles dá vantaxe, a célula morre".
Na sección de Rodríguez, por exemplo, investigaban aos inhibidores do EGFRa. O EGFR é un receptor situado na superficie celular ( epidermal growth factor receptor ) que controla que o xene que o controla estea mutado ou que a súa expresión sexa excesiva pode causar cancro. "O bloqueo da sinalización de EGFR impide o desenvolvemento do cancro. Pois os inhibidores probados por nós xa se utilizan nos pacientes. Uno deles é o erlotinib, utilizado nos hospitais paira tratar os cancros de pulmón". Tamén se están probando moléculas anti-COVs, o propio erlotinib ou outros inhibidores en cerebro, colon e outros tipos de cancro, dependendo do mecanismo de cada tipo de tumor.
Hai que ter en conta que hai moitos tipos de cancro. "Moitos din que cada paciente ten un tipo de cancro, o seu", di Rodríguez. Por iso, os investigadores deben buscar os inhibidores máis adecuados de todos os cancros. Paira iso é necesario analizar os defectos xenéticos (mutacións) que orixinaron o tumor.
A guerra ás resistencias
En calquera caso, Rodríguez advirte que esta estratexia ten un límite: "O problema é que desenvolven resistencias aos inhibidores".
Co tempo, cando inhibimos una senda, as células tumorales empezan a utilizar outras sendas que serven paira facer o mesmo e vólvense resistentes ao inhibidor. Por iso, deben administrarse de forma combinada.
En palabras de Rodríguez, "esta é una guerra, e cando se pecha un camiño debemos tentar por outro". Ademais da vía dos inhibidores das sendas, tamén é importante a dos anticorpos monoclonales. Inclúe, por exemplo, trastuzumab (Herceptina), anticorpo contra un receptor similar ao EGFR. Trastuzumab utilízase habitualmente contra o cancro de mama e agora tamén está a probar en ensaios clínicos outros tipos de cancro.

Estes anticorpos xéranse no laboratorio e son capaces de unirse especificamente a un antígeno concreto. Os anticorpos monoclonales foron utilizados desde hai tempo no diagnóstico do cancro. A modo de terapia, os investigadores tentan identificar na superficie das células tumorales os antígenos relacionados co crecemento (p.ex. receptores de factores de crecemento) e deseñar os anticorpos asociados a eles. Desta forma, os anticorpos únense aos antígenos e as células non poden crecer.
Tamén se utilizan anticorpos monoclonales deseñados especificamente paira o fomento do sistema inmunitario.
Vacinas contra o cancro
En relación ao sistema inmunitario, outra das vías que se están investigando paira combater o cancro é a vacinación.
As vacinas utilizadas en enfermidades infecciosas adminístranse antes da aparición da enfermidade. Estas vacinas conteñen fragmentos de antígenos do axente infeccioso ou desactivados polo mesmo axente e teñen como obxectivo preparar o sistema inmunitario cando o axente entra no corpo. Dalgunha maneira, as vacinas ensínanlle quen é o agresor, o que permite ao corpo preparar as mellores armas contra el.
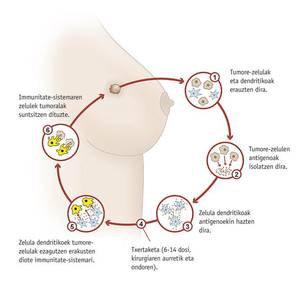
As vacinas contra o cancro, con todo, utilizaríanse despois da aparición da enfermidade paira tratala ou impedir a súa difusión. Uno deles está a ser probado na Clínica Universidade de Navarra. O obxectivo da vacina é evitar a aparición dun cancro de mama despois de ser tratado e paira iso utilízanse células dendríticas da muller (células do sistema inmunitario) que son estimuladas con células tumorales do propio paciente. Así ensinan ás células dendríticas cal é o agresor.
Marta Santisteban, xefa de investigación, sinalou que se está probando cun subgrupo de pacientes con cancro de mama e que saberán si é efectivo en maio de 2012. En calquera caso, complementaría a terapia convencional oncolóxica e non a cirurxía, a radioterapia e a quimioterapia.
Ademais da loita contra o cancro de mama, tamén se están probando vacúas paira outros cancros noutros cultivos como o de próstata, ril, ovario, colon...
Con todo, Rodríguez considera que aínda que se demostre que as vacinas son efectivas, será difícil que a molécula se converta en inhibidora e convencional. "A cuestión é que son autólogos, é dicir, que se fan con células do propio paciente. Por tanto, cada un ten que facer o seu, e iso non está ao alcance de todos, porque é moi caro".
Virus, cabalo de Troia
Outra estratexia que está a dar bos resultados é a dos virus. Rodríguez explica en que consiste: "Tentan transformar o xenoma dos virus para que poidan destruír as células tumorales sen destruír as células normais. Son frecuentes os virus oncolíticos. A estes virus modificáronselles os xenes para que só poidan entrar nas células tumorales. Ao entrar nunha célula tumoral, os virus non fan máis que dividilos unha e outra vez ata que a célula explota".
Noutras ocasións introdúcese un xene que codifica un tóxico. "Deste xeito, una vez introducidas na célula, producen o tóxico e matan activamente á célula. Armed viruses". Os virus armados.
Os virus oncolíticos e armados son exemplos de terapia génica e as súas investigacións e ensaios clínicos están bastante avanzados. Outros que se están probando na barra de terapia génica atópanse en fases posteriores. Entre eles atópanse os ensaios de substitución de xenes mutados en células por xenes sans. Noutros laboratorios inclúense xenes específicos en células tumorales paira ser máis sensibles á radioterapia e á quimioterapia. Tamén hai quen tentan introducir xenes que impiden a angiogénesis, cos que os tumores non poden producir e difundir vasos sanguíneos.
Son moitos os camiños que están a probar os investigadores. Algúns aínda están en fase experimental, pero outros xa están moi avanzados e foron autorizados paira o seu uso. Hai cada vez máis oportunidades que abren o camiño á esperanza.