Proteinak birziklatzea, osasuntsu egoteko giltza
2020/03/01 Osinalde Moraleja, Nerea - EHUko Biokimika eta Biologia Molekularra Saileko irakaslea | Elu Arantzamendi, Nagore - EHUko ikertzailea Iturria: Elhuyar aldizkaria
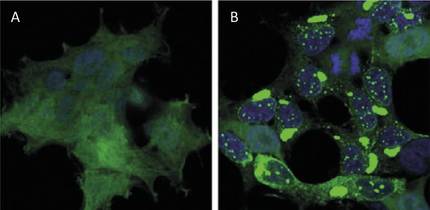
Hondakinak birziklatzeak mundu mailan duen inpaktuaren parekoa dauka zelula mailan proteinak birziklatzeak. Proteinak dira zelulen funtzionamendua bermatzen duten molekula nagusiak. Haien ardura da, besteak beste, erreakzio kimikoak gauzatzea, geneak erregulatzea, molekulak garraiatzea eta zelulen egitura mantentzea. Zelula bakoitzak milaka proteina ditu, eta, gainera, oso era dinamikoan osatzen dira proteinak. Izan ere, unean uneko zelularen beharrei edo kanpoko estimuluei erantzuteko, etengabe ari da zelula mota askotako proteinak ekoizten eta deuseztatzen. Hortaz, ezinbestekoa da aurkako bi prozesu horien arteko oreka mantentzea, zelularen funtzionamendu zuzena bermatzeko. Horregatik, ez da harritzekoa gure gizartea gogor astintzen duten gaixotasun askoren jatorrian egotea proteinen sintesi- eta degradazio-prozesuen desorekak. Proteinen pilaketa patologikoaren ondorioz garatutako gaitzen artean ditugu, esaterako, alzheimerra, parkinsona eta huntingtona, guztiak ere aski ezagunak [1,2] (1. irudia).
Proteinak: egokiro tolestu ala akabo!
Proteinak ekoizteko informazioa geneetan dago gordeta. DNA-katean dago zehaztuta noiz eta zer proteina sortuko den. Proteinen ekoizpen-fabrikatik, alegia, erribosometatik ateratzen den proteina baten egitura perlazko lepoko baten parekoa da, perlak aminoazidoak izanik. Alabaina, proteina horrek, funtzionala izateko, hiru dimentsioko egitura jakin bat izan behar du. Zelulan 20 aminoazido-mota aurkitu ditzakegu, eta proteina bakoitzaren aminoazido-sekuentziak zehazten du zein izango den proteina horren hiru dimentsioko egitura funtzionala, hots, egitura natiboa. Zeluletako baldintzak oso bereziak dira, eta, ondorioz, proteinek egitura natiboa lortzeko, txaperoi molekular izeneko proteinen laguntza behar izaten dute maiz. Gizakiok ehundik gora txaperoi ditugu, eta horietako bakoitza ehunka itu-proteinaren toleste-prozesuaz arduratzen da. Mutazioen ondorioz txaperoien jarduera kaltetuta dagoenean, itu-proteinen toleste-prozesua ez da egokia izaten, eta, ondorioz, proteina horiek ez dira funtzionalak izaten. Degradatzen ez badira, zelulan pilatzen dira eta kalte larriak eragiten dituzte [4] (2. irudia).
Adibidez, HSPB1 deituriko txaperoian gertatutako mutazioek alboko esklerosi amiotrofikoa eta Charcot Marie Tooth izeneko neuropatia larria eragiten dute [5,6]. Eta CHIP txaperoia mutatuta daukatenek Gordon Holmes sindromea garatzen dute, hipogonadismoa eta arazo neurologikoak eragiten dituen gaitz bakana.
Baina proteinak gaizki tolestu eta ondorioz patologikoki pilatzen diren kasu guztietan, errua ez da txaperoiena. Kasu batzuetan, genoman gertatzen diren mutazioak tarteko, proteinak behar baino aminoazido gehiagorekin ekoizten dira, eta horrek eragotzi egiten du proteinak dagokion egitura natiboa lortzea (2. irudia).
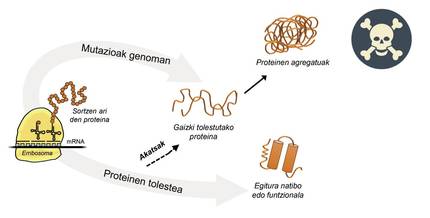
Esaterako, huntington gaixotasuna pairatzen dutenek huntingtina proteina akastuna daukate. Izan ere, huntingtina kodetzen duen HTT genea mutatzen denean, ekoitzitako proteinak behar baino glutamina aminoazido gehiago ditu, hau da, perla jakin baten ale gehiegi ditu [4]. Alboko esklerosi anizkoitza eta dementzia frontotenporala pairatzen dutenek ere behar baino glizina-alanina aminoazido bikote gehiago dituen C9orf72 proteina akastuna dute, zeinak joera handia baitu neuronetan pilatzeko [7].
Edonola ere, proteinen pilaketek eragindako gaitz ezagunena alzheimerra da, gaur egungo gizartea gogor astintzen duen gaitza. Burmuinean dagoen hipokanpoko neuronak hiltzen zaizkien heinean, gaixoek gaitasun kognitiboak galtzen dituzte, bereziki epe laburreko memoria. Baina, zergatik hiltzen dira neuronak? Gero eta ebidentzia gehiago dago pentsatzeko tau proteina eta beta-amiloide proteina mutatuen pilaketak direla neuronen heriotzaren erantzule nagusiak [6].
Proteasoma: proteina-birringailua
Eta zelulak ez al dauka mekanismorik gaizki tolestutako proteinak degradatu eta agregatu patologikoak saihesteko? Bai, eta bat baino gehiago gainera. Baina, batetik, arestian aipatutako adibideak aintzat hartuta, bistakoa da proteina-pilaketa batzuk gai direla mekanismo horiei muzin egiteko; eta, bestetik, proteinak degradatzeko makinariak berak ere arazoak izan ditzake, eta birziklatze-prozesua eragotzi.
Gaizki tolestutako proteinak ez ezik, zelularentzat erabilgarri ez diren proteina gehienak ere proteasoma izeneko konplexu multiproteiko bati esker degradatzen dira. Baina zelulan dauden milaka proteinen artean, nola jakin daiteke zein den degradatu behar dena? Nola hautematen ditu proteasomak zer proteina txikitu behar diren? Bada, ubikuitina izeneko molekula txiki bat itsatsia dutelako. “Proteasomara joan behar duzu degradatzera” dioen post-it bat balitz bezala funtzionatzen du molekula horrek. Proteasoma, berriz, paper-birringailu baten pare aritzen da. Proteinak txikitzen ditu, hots, aminoazidoen arteko loturak apurtzen ditu. Horrekin batera, zelularentzat eskuragarri jartzen ditu aminoazido askeak, molekula berriak ekoizteko [8]. Hori dela eta, esan daiteke proteasomak proteinak birziklatzen dituela (3. irudia).
Proteinen birziklapen-prozesua oso konplexua da, eta nahikoa da edozein puntutan akats bat gertatzea gaixotasun bat gara dadin. Proteasomara bideratu behar diren proteinei ubikuitina lotzeko prozesuan, hiru entzima-mota aritzen dira elkarlanean: E1, E2 eta E3 entzimak. Baldin eta entzima horiek mutatuta egoteagatik proteinen ubikuitinazio-prozesua ez bada zuzena, degradatu beharreko proteinak ez dira deuseztatzen, eta zelulan pilatzen dira. Toxikotasun hori batez ere oso kalteberak diren neuronetan nabarmentzen da, eta horrek esan nahi du gaixotasun neurologiko askok erlazioa dutela entzima horietan gertatzen diren akatsekin [8].
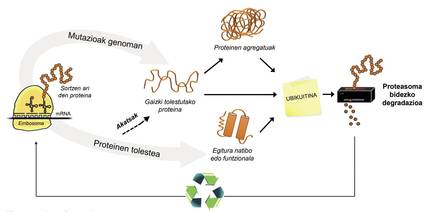
E1 motako UBA1 entzima, adibidez, soilik mutilei eragiten dien ezohiko gaixotasun neuromuskular batekin dago erlazionatuta. Gaixo horiek, giharretan ahulezia handia izateaz gain, ez daukate erreflexurik, hau da, giharrek ez dute behar bezala erantzuten kanpo-estimuluen aurrean. E2 motako UBE2A entzima mutatuta daukatenek, berriz, UBE2A urritasunaren sindromea garatzen dute, ezohiko gaitz neurologikoa. Gaixotasun hori ere soilik gizonezkoek pairatzen dute, eta hauek dira sintoma ohikoenak: adimen-urritasuna, azaleko nahiz ugal- eta gernu-aparatuko nahasmenduak eta mintzamenik eza.
Proteinen ubikitinazioa gauzatzen duten hiru entzimen artean E3ak dira ugarienak. Hori horrela, E3 entzima mutaturen bat dago ubikuitinazio akastunaren ondorioz garatutako gaitz neurologiko gehienen atzean. Adibidez, autismoaren espektroko nahasmenduen barruan sailkatutako familiako autismoa eta noizbehinkako autismoa pairatzen dutenek E3 motako UBE3B eta UBE3C entzimak dauzkate mutatuta, hurrenez hurren. Aitzitik, UBE3A akastuna dutenek autismoarekin erlazionatuta dagoen Angelmanen sindromea garatzen dute [9].
Autismoarekin erlazionatutako gaitzez gain, mutatutako E3ek oso bestelako gaitz neurologikoak eragin ditzakete. Adibidez, gigaxonina izeneko E3 entzima mutatuta daukatenek axoi erraldoien neuropatia garatzen dute. Baldintza osasuntsuetan, gigaxoninak neurona-besoen, hots, axoien neurofilamentuak ubikuitinatzen ditu, eta axoi horien egitura eta tamaina baldintzatzen. Gigaxonina mutatzen denean, ordea, ez-funtzional bilakatzen da, eta ez ditu axoien neurofilamentuak ubikuitinatzen. Horrek eragiten du neurofilamentuak ez degradatzea, eta neuronen axoiak behar baino handiagoak eta luzeagoak izatea. Ondorioz, neuropatia hori pairatzen duten gaixo gehienek arazoak izaten dituzte ibiltzeko eta, oro har, mugimenduak koordinatzeko [9].
Berriki deskribatu duten Tenorioren sindromearen atzean ere E3 entzima bat dago; kasu horretan, RNF125 izenekoa. Tenorioren sindromeak jota daudenek adimen-urritasuna daukate. Gainera, gehiegizko hazkuntza —bereziki garezurra neurriz gain garatzea— da gaixo horien bereizgarria. Kontrakoa gertatzen zaie TRIM36 mutatuta daukatenei; izan ere, gaixo horiei garezurraren eta garunaren zati handi bat falta zaie [9].

Ondorioak
Bistakoa da proteinen sintesi- eta degradazio-szikloan desoreka gertatuz gero ondorio benetan kaltegarriak izan ditzaketela zelulek eta, oro har, organismo bizidunek. Alde batetik, mutazioen ondorioz gaizki tolestutako proteinek, zabor-poltsa erabilezinak balira bezala pilatuta, zelulen heriotza eragin dezakete. Bestalde, proteinak degradatzeaz eta birziklatzeaz arduratzen diren gailu molekularrak hondatzen direnean, proteinen pilaketa toxikoak gertatzen dira. Hain zuzen ere, hondakinak birziklatzeko instalazio baten jarduera bertan behera geratuko balitz zaborra metatuko litzatekeen antzera.
Badakigu egungo gizartearen erronka nagusietako bat dela hondakinak behar bezala kudeatzea. Izan ere, hondakinen birziklapena bermatu ezean, gure ozeano eta soroak zaborrez estaliko ditugu urte gutxitan, eta bizitza jasangaitza bilakatuko da. Mundu mikroskopikoan ere zelulek erronka bertsua dute, funtzionalak ez diren proteinak kudeatzeko arazoak dituztenean. Beren osasuna bermatzeko, ezinbestean deuseztatu behar dituzte proteina toxikoak.
Beraz, hurrengoan zure etxeko hondakinak birziklatzea ahazten bazaizu, gogoan izan zelula batentzat nolako hondamendia ekarriko lukeen horrek. Izan ere, gizakiok sortzen dugun zaborra birziklatzea eta zeluletan pilatzen diren proteinak birziklatzea ekintza berdintsuak dira, eskala handian eta txikian. Guztiok osasuntsu mantentzeko giltza.
Bibliografia




