Titanioa, baterien barneko kuxin egonkortzailea
2020/03/01 Lakuntza Irigoien, Oier - Kimikan doktoreaKimika Teorikoko Laborategia Iturria: Elhuyar aldizkaria
Litio-ioizko bateriak (LIB) giltzarri izan ziren gailu eramangarri, ibilgailu elektriko eta energia berriztagarrien garapenean. Gaur egun, ordea, ezbaian jartzen dute iraultza hori litioaren eskuragarritasun ezak, munduan litioak duen banaketa desorekatuak eta bateria-mota hauetan nikela (Ni) eta kobaltoa (Co) erabiltzeak dakartzan ingurumen-kalteak.
Azken urteotako garapenari esker, kostua eta lehengaien eskuragarritasuna garrantzitsuak izanik, ikusi da sodio-ioizko bateriak (NIB) LIBen ordezko izatera irits daitezkeela. Hala, oso interesgarri bihurtu dira sodio- eta manganeso-oxido laminarrak (Na eta Mn, hurrenez hurren), Co eta Ni gabekoak.
Interes hori zor zaio, hein handi batean, aldeko prozesu elektrokimikoei eta trantsizio-metal elektroaktibo nagusia Mn-a izateari. Azken batean, Mn-a elementu eskuragarria, garbia eta merkea da, eta, oxidazio-egoera bat baino gehiago izanik, aukera ematen du erredox-potentziala nahi bezala egokitzeko konposatuak sintetizatzeko (Mn3+/Mn4+ da gehien erabiltzen den parea).
Ikusi ahal izan denez, oxido laminar horiek titanioz (Ti) dopatzean, baterien iraunkortasuna hobetzen da, eta karga/deskarga ziklo bakoitzean kapazitatea hobeto mantentzea eragin dezake. Dena den, titanioak horretan jokatzen duen papera azaldu aurretik, ikus dezagun oxido laminarren egitura zein den eta zer arazo nagusi izaten dituzten.
Sandwich-formako osagaiak
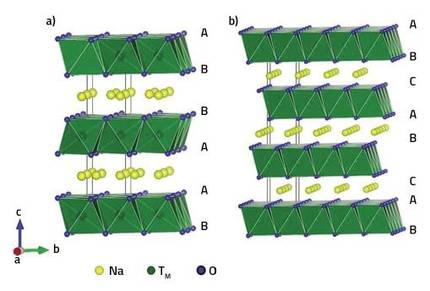
Sodio-ioizko baterien katodoetarako erabiltzen diren oxido laminarretan, oxigenoz, trantsizio-metalez eta sodioz osatutako geruzak bereiz daitezke. Bi oxigeno-geruzen arteko hutsune oktaedrikoetan kokatzen dira trantsizio-metalak, eta oxigeno arteko gainerako hutsuneak betetzen dituzte sodio-atomoek. Hala, sodio-atomoak kokatzen diren hutsuneen arabera, P eta O motako egiturak bereizten dira: P esaten zaie sodio-atomoak prisma trigonaletan daudenean, eta O, hutsune oktaedrikoetan daudenean. Era berean, izenean zenbakiak erabiltzen dira, adierazten dutenak egitura osoa deskribatzeko zenbat sodio-geruza behar diren. Hala, P2, O2 eta O3 motako egiturak izan ditzakegu, betiere, oxigeno-geruzen kokapen erlatiboaren arabera.
Ikerketek erakutsi dutenez, P egiturak O egiturak baino egokiagoak dira baterien katodoetarako, sodio-atomoak errazago mugitzen baitira prisma batetik bestera, oktaedro batetik bestera baino. Edonola ere, erabilitako baldintzen eta sodio-kantitatearen arabera, P→O transformazioak gertatzen dira, eta horrek bateriaren karga/deskarga prozesua mugatzen du.
Manganesoa, elementu aktiboa
Manganeso-oxido laminarretan, Mn-a izaten da elementu aktiboa. Alegia, bateria kargatzeko/deskargatzeko prozesuan, sodioak oxido laminarretik atera/sartzen direnean, manganesoak hartzen/askatzen ditu sodioaren elektroiak, Mn3+/Mn4+ bihurtuz. Hain zuzen ere, hori da oxido laminar horien arazo nagusiaren sorburua. Izan ere, Mn4+-ak ez bezala, Mn3+-ak, bere elektroi konfigurazioa dela medio, Jahn-Teller (JT) distortsioa pairatzen du. Horren ondorioz, manganesoaren inguruko sei oxigenoek osatzen duten oktaedroa luzatu eta laburtu egiten da, eta, kontuan izanik karga/deskarga ziklo bakoitzean Mn3+→Mn4+→Mn3+ eraldaketa gertatzen dela, horrek kalte egiten dio oxido laminarrari zikloz ziklo.
Arazo horri aurre egiteko, oxido laminarrak elementu ez-aktiboz dopatzen dira, alegia, bateria kargatzeko/deskargatzeko prozesuan elektroiak hartzen/askatzen ez dituzten elementuz, adibidez, magnesioa eta titanioa. Ildo horretan, CIC EnergiGUNEko ikertzaile batzuek ikerketa bat egin genuen Na2/3Fe0,2Mn0,8O2 konposatuan oinarrituta, alegia, kondizio elektrokimikorik aldekoenak lortzen dituen burdin eta manganeso-oxido laminarrean oinarrituta. Ikerketan ikusi genuenez, konposatu hori titanio-kantitate ezberdinez dopatzean, zikloz ziklo kapazitatearen bilakaera aldatu egiten zen. Berriki, Journal of Material Chemistry A aldizkarian argitaratu dugun lan batean azaldu dugu zer paper duen titanioak horretan; neurketa elektrokimikoak, X izpien absortzio espektroskopia eta dentsitate funtzionalaren teoria (DFT) erabiliz egindako kalkulu teorikoak uztartu ditugu hori azaltzeko.
Laburbilduz, esan daiteke titanioa gai dela inguruko metal aktiboen (manganesoa, kasu honetan) oktaedroen distortsioak absorbatzeko. Hau da, elektroi-konfigurazioak JT distortsiorik eragin ez arren, titanioa gai da bere oktaedroa moldatuz inguruko distortsioetara egokitzeko. Funtsean, titanio-oxigeno lotura ahulagoa izaki, inguruko mugimenduetara egokituz, kuxin baten moduan jokatzen du metal horrek egituran, eta, hala, gai da egitura osoari egonkortasuna emateko.
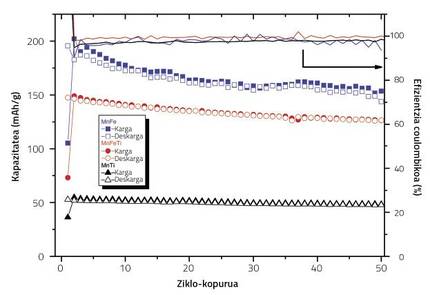
Edonola ere, titanio-kontzentrazioa egoki zaindu beharra dago. Ikerketa Na2/3Fe0,2Mn0,8O2-an oinarritu genuen, hori baita burdin eta manganeso-oxido laminarren artean kondizio elektrokimikorik egokiena lortzen duena. Ikerketan, hiru titanio-kontzentrazio erabili genituen, eta horietako batekin soilik lortu ziren emaitza egokiak. Titaniorik erabili ezean, kargatze-/deskargatze-zikloak egin ahala, katodoaren kapazitateak nabarmen egiten zuen behera. Konposatuaren burdin guztia titanioz ordezkatzen genuenean, hasierako kapazitatea asko jaisten zen. Aldiz, burdinaren erdia titanioz ordezkatu genuenean, hasierako kapazitatea egokia zen, baita zikloz ziklo zuen bilakaera ere. Izan ere, titanio-kontzentrazioa igo ahala, handitu egiten da haren oktaedroen luzatzea/laburtzea pairatzen duten Mn3+-en kontzentrazioa ere, eta horrek eragiten du bateriaren kapazitatea hasieratik txikia izatea. Dopatzailearen kontzentrazioa txikiagoa denean, aldiz, Mn3+ gutxiago egongo da konposatuan, eta hasierako kapazitatea altuagoa izateaz gain, egituran dagoen titanioaren kuxin-izaerak ahalbidetzen du kapazitatea hobeto mantentzea zikloz ziklo.
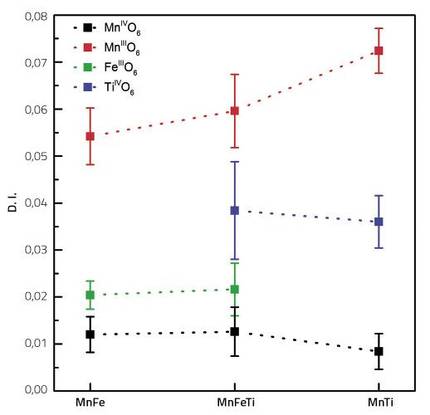
Aipaturiko izaera hori islatzeko, konposatuko trantsizio-metal guztien (Fe, Ti, Mn3+ eta Mn4+) distortsio-indizeak kalkulatu genituen teorikoki. Indize horrek adierazten digu zenbat urruntzen den trantsizio-metalaren atomo bakoitzaren inguruko sei oxigenoek osatzen duten poliedroa oktaedro erregular batetik.
Hala, azterturiko hiru konposatuen kasuan, Mn3+ katioia zen distortsio-indizerik handiena zuena. Beste muturrean Mn4+ zegoen, oktaedro erregular batetik gertuen gelditzen zena, alegia. Hori erraz uler daiteke kontuan hartzen badugu Mn3+ katioiak JT distortsioa pairatzen duela bere elektroi-konfigurazioa dela-eta.
Deigarriena, ordea, Ti eta Fe-aren arteko diferentzia da. Izan ere, titanioaren distortsio-indizea burdinarena baino bi edo hiru aldiz handiagoa da. Funtsean, bi trantsizio-metal horiek berez ez lukete distortsiorik izan behar, beren elektroi-konfigurazioak ez baitie halakorik eragiten. Bi metal ez-aktibo horien distortsioa inguruko oktaedroen distortsioen eragina baino ez da. Hala, titanioaren indizea burdinarena halako bi edo hiru izateak adierazten du titanioak hobeto egokitzen dituela inguruko distortsioak burdinak baino. Alegia, katodoaren osagai ez-aktiboak kuxin batekin alderatzen baditugu, beren distortsio-indizeak kuxin horren biguntasun-maila adieraziko luke. Zenbat eta distortsio-indize handiagoa izan, orduan eta kuxin malguagoa izango dugu, eta horri esker errazago absorbatuko ditu inguruko oktaedroen irregulartasunak.
Pausoz pauso…
Lan hartan ikusi ahal izan genuenez, balizko sodio-ioizko baterien iraupena hobetzen lagundu lezake titanioak. Alegia, bateria-mota hori lerabilkeen ordenagailu eramangarri edo ibilgailu elektrikoa maizago kargatu ahal izango genuke, bere bateriaren kapazitatea gehiegi kaltetu gabe.
Edonola ere, sodio-ioizko baterien bidean beste pauso txiki bat baino ez da hau. Ikusteke dago titanioa ez den beste dopatzaile batzuek nolako eragina luketen. Esate baterako, ikusi ahal izan denez, batzuetan oso emaitza interesgarriak lortzen dira dopatzaile gisa zinka erabiltzen denean ere, eta horren arrazoia oraindik ez da oso ongi ulertzen.
Halaber, P2 motako oxido laminarretan, trantsizio-metalen oktaedroekin aurpegiren bat elkarbanatzen duten prismetan sodioren bat aurkitzen denean, ikusi da P2→O2 transformazioa zailtzen dela. Horrek bateria kargatzeko/deskargatzeko prozesua errazten du. Beraz, dopatzaileaz gain, kontuan hartu beharko da sodio-atomoen kokapenak zer funtzio izan dezakeen ere.
Ikerketa horietan guztietan dihardugu CIC EnergiGUNEko sodio-ioizko baterien lerroko hainbat ikerketa-taldek.
Bibliografia