Titane, coussin stabilisateur intérieur de batteries
2020/03/01 Lakuntza Irigoien, Oier - Kimikan doktoreaKimika Teorikoko Laborategia Iturria: Elhuyar aldizkaria
Les batteries ion-lithium (VOL) ont joué un rôle clé dans le développement d'appareils portables, de véhicules électriques et d'énergies renouvelables. Aujourd'hui, cependant, l'indisponibilité du lithium, la distribution inégale du lithium dans le monde et les dommages environnementaux découlant de l'utilisation du nickel (Ni) et du cobalt (Co) dans ce type de batteries mettent en doute cette révolution.
En raison du développement de ces dernières années, le coût et la disponibilité des matières premières sont importants, il a été prouvé que les batteries de sodium ion (NIB) peuvent être substituées aux OPS. Ainsi, les oxydes lamellaires de sodium et de manganèse (Na et Mn respectivement), sans Co et sans Ni, sont devenus très intéressants.
Cet intérêt est dû en grande partie aux processus électrochimiques favorables et au fait que le principal métal de transition électroactif est le Mn. En définitive, le Mn est un élément abordable, propre et bon marché qui, avec plus d'une situation d'oxydation, permet la synthèse des composés pour l'adaptation souhaitée du potentiel redox (la paire la plus utilisée est Mn3+/Mn4+).
On a pu constater que le dopage de ces oxydes laminés au titane (Ti) améliore la durabilité des batteries et peut entraîner un meilleur maintien de la capacité dans chaque cycle de charge/décharge. Mais avant d'expliquer le rôle joué par le titane, voyons quelle est la structure des oxydes laminés et quels sont leurs principaux problèmes.
Composants sandwich
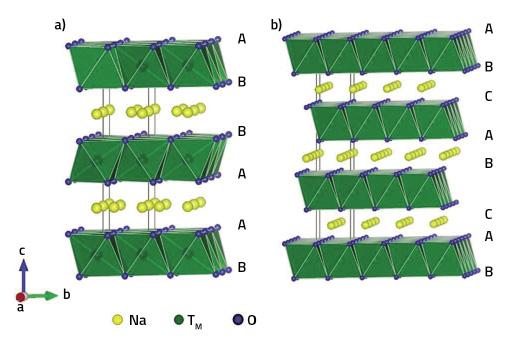
Les oxydes laminés utilisés pour les cathodes de batteries de sodium ion peuvent distinguer les couches d'oxygène, les métaux de transition et de sodium. Les métaux de transition sont situés dans les cavités octaédriques entre les deux couches d'oxygène, occupant le reste des cavités interoxygéniques. Ainsi, en fonction des trous dans lesquels se trouvent les atomes de sodium, on distingue les structures type P et type O: Ils sont appelés P lorsque les atomes de sodium se trouvent dans des prismes trigonales et O lorsqu'ils sont dans des cavités octaédriques. Des nombres sont également utilisés dans le nom indiquant le nombre de couches de sodium nécessaires pour décrire toute la structure. Les structures P2, O2 et O3 peuvent ainsi être disponibles en fonction de la position relative des couches d'oxygène.
Des études montrent que les structures P sont plus appropriées pour les cathodes des batteries que les structures O, puisque les atomes de sodium se déplacent plus facilement d'un prisme à l'autre que d'un octaèdre à l'autre. Toutefois, en fonction des conditions et de la quantité de sodium utilisées, des transformations de P O se produisent, ce qui limite le processus de chargement/déchargement de la batterie.
Manganèse, élément actif
Dans les oxydes lamellaires de manganèse, l'élément actif est le Mn. C'est-à-dire, pendant le processus de charge/décharge de la batterie, lorsque les sodium sont extraits/introduits de l'oxyde laminaire, le manganèse capte/libère les électrons du sodium, devenant Mn3+/Mn4+. C'est le principal problème de ces oxydes lamins. Contrairement à Mn4+, Mn3+ souffre d'une distorsion de Jahn-Teller (JT) en raison de sa configuration électronique. En conséquence, l'octaèdre formé par les six oxygènes autour du manganèse s'allonge et se raccourcit, et étant donné que dans chaque cycle de charge/décharge se produit la transformation de Mn3+{ Mn4+ Mn3+, ce qui affecte négativement l'oxyde laminaire pendant des cycles.
Pour faire face à ce problème, les oxydes lamellaires sont dopés avec des éléments inactifs, tels que le magnésium et le titane, qui ne captent pas/libèrent des électrons pendant le processus de charge/décharge de la batterie. En ce sens, des chercheurs de CIC EnergiGUNE ont réalisé une étude basée sur le composé Na2/3Fe0,2 Mn0.8O2, qui est l'oxyde laminaire de fer et de manganèse qui obtient les conditions électrochimiques les plus favorables. Dans l'étude, nous avons constaté qu'en dopant ce composé avec différentes quantités de titane, l'évolution de la capacité de cycle à cycle changeait. Récemment, dans un ouvrage publié dans le Journal of Material Chemistry A, nous avons expliqué le rôle du titane dans ce sens, combinant des mesures électrochimiques, la spectroscopie d'absorption de rayons X et des calculs théoriques en utilisant la théorie de la densité fonctionnelle (DFT).
En résumé, on peut dire que le titane est capable d'absorber les distorsions d'octaèdres des métaux actifs de la zone, dans ce cas le manganèse. Si la configuration électronique ne produit pas de distorsions JT, le titane peut adapter son octaèdre aux distorsions de l'environnement. En substance, étant plus faible l'union titane-oxygène, s'adaptant aux mouvements de l'environnement, ce métal se comporte dans la structure comme un coussin capable de donner la stabilité à toute la structure.
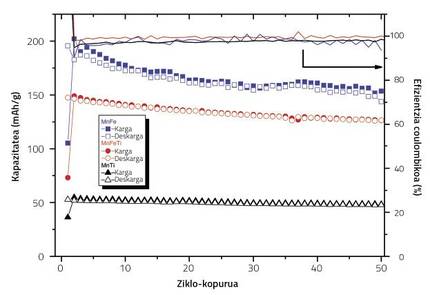
Dans tous les cas, la concentration en titane doit être bien entretenue. L'étude a été basée sur le Na2/3Fe0,2 Mn350O2, qui est celui qui obtient le meilleur état électrochimique entre les oxydes laminés de fer et de manganèse. Dans la recherche, nous utilisons trois concentrations de titane, dont seuls des résultats satisfaisants ont été obtenus. En l'absence de titane, au fur et à mesure des cycles de chargement/déchargement, la capacité de la cathode diminuait considérablement. Quand on remplaçait tout le fer du composé par du titane, la capacité initiale diminuait considérablement. En revanche, lorsque nous avons remplacé la moitié du fer par du titane, la capacité initiale était appropriée, ainsi que son évolution cycle par cycle. En effet, à mesure que la concentration de titane augmente, la concentration de Mn3+ souffre d'étirement/raccourcissement de ses octaèdres, ce qui rend la capacité de la batterie faible dès le début. Cependant, lorsque la concentration du dopant est moindre, Mn3+ sera moins dans le composé, et en plus d'avoir une capacité initiale plus élevée, la lame du titane dans la structure permet de mieux maintenir la capacité cycle à cycle.
Comme reflet de ce caractère, nous calculons théoriquement les taux de distorsion de tous les métaux de transition du composé (Fe, Ti, Mn3+ et Mn4+). Cet index nous indique combien il s'éloigne d'un octaèdre régulier formé par six oxygènes autour de chaque atome du métal de transition.
Ainsi, pour les trois composés analysés, le cation Mn3+ présentait le taux de distorsion le plus élevé. À l'autre extrémité se trouvait Mn4+, le plus proche d'un octaèdre régulier. Ceci est facilement compréhensible si l'on considère que le cation Mn3+ est déformée par sa configuration électronique.
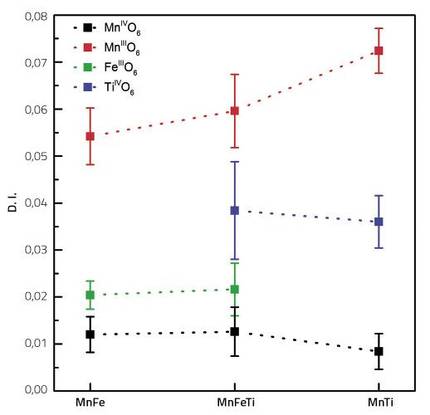
Le plus frappant est la différence entre Toi et Foi. Le taux de distorsion du titane est deux à trois fois supérieur à celui du fer. Fondamentalement, ces deux métaux de transition ne devraient pas présenter eux-mêmes distorsions, car leur configuration électronique ne les affecte pas. La distorsion de ces deux métaux inactifs est due uniquement aux distorsions des octaèdres environnants. Ainsi, le fait que l'indice de titane soit deux ou trois fois supérieur à celui du fer indique que le titane adapte mieux les distorsions de la zone que le fer. Autrement dit, si nous comparons les composants inactifs de la cathode à un coussin, son indice de distorsion indiquerait le degré de relâchement du coussin. Plus le taux de distorsion est élevé, plus le coussin est flexible, ce qui facilitera l'absorption des irrégularités des octaèdres environnants.
Pas à pas…
Dans ce travail, nous avons pu vérifier que le titane pourrait améliorer la durée des batteries de sodium ion possibles. Autrement dit, nous pourrions charger plus souvent le portable ou le véhicule électrique utilisant ce type de batteries sans trop endommager la capacité de votre batterie.
Cependant, c'est un petit pas de plus sur le chemin des batteries de sodium ion. C'est pour voir comment d'autres dopants autres que le titane seraient affectés. Par exemple, on a pu constater que parfois on obtient des résultats très intéressants même lorsqu'on utilise du zinc comme dopeur, ce qui n'est pas encore très bien compris.
De même, dans les oxydes lamellaires de type P2, lorsqu'on détecte la présence de sodium dans des prismes partageant une face avec des octaèdres de métaux de transition, on a observé que la transformation P2 O2 était compliquée. Cela facilite le processus de chargement/déchargement de la batterie. Ainsi, en plus du dopant, il faudra tenir compte de la fonction qui peut avoir la position des atomes de sodium.
Toutes ces recherches impliquent différents groupes de recherche de la ligne de batteries de sodium ion de CIC EnergiGUNE.
Bibliographie Bibliographie




