Zelula amak: etorkizuneko biomedikuntzaren eragileak
2021/07/12 Ainhoa González Pujana - EHUko NanoBioCel taldeko ikertzailea | Rosa María Hernández Martín - EHUko NanoBioCel taldeko ikertzailea | Edorta Santos Vizcaíno - EHUko NanoBioCel taldeko ikertzailea Iturria: Elhuyar aldizkaria
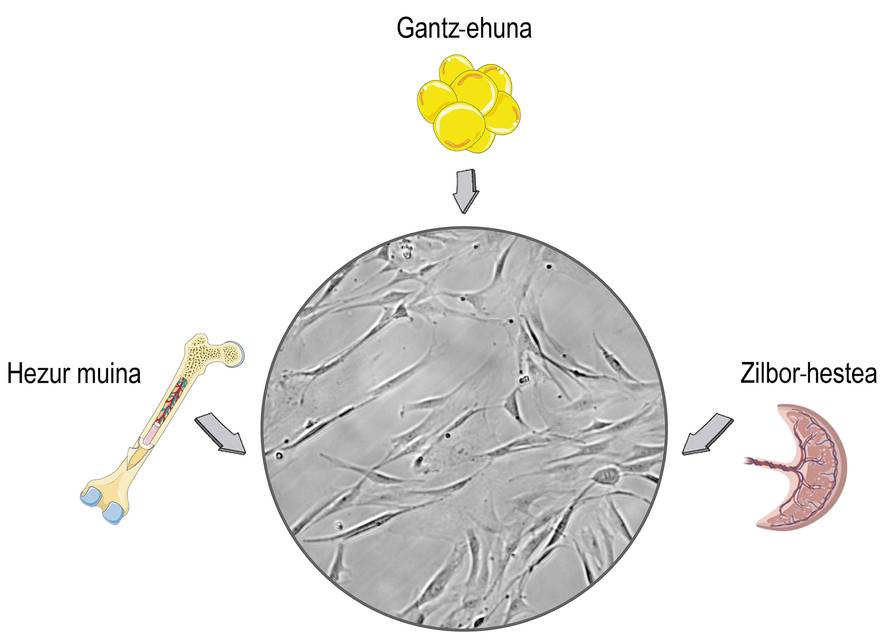
Zer dira zelula amak eta zer efektu terapeutiko dituzte?
Zelula amak ugaztunen ehun estromaletan aurkitzen diren zelulak dira. Segur aski, haien erabilera eztabaida etiko eta erlijiosoekin lotzen duzu, eta kezka hori haien jatorriarekin erlazionatuta dago. Zelula amak ehun enbrionarioetatik isola daitezke, eta horrek arazo moralak ekar ditzake. Kontua da zelula amak organismo helduetatik ere lor ditzakegula, eta arazo horiek alde batera utzi. Ondorioz, ikerketa gehienetan emaile helduetatik isolatzen dira zelula amak, gehienbat zilbor-hestetik, hezur-muinetik eta gantz-ehunetik (1. irudia).
Zelula horiek erabiltzearen motibazio nagusia ezaugarri terapeutikoak dira. Haien artean, beste zelula-mota batzuetara eraldatzeko duten ahalmena da ezagunena. Zenbat zelula-motatan bereizi daitezkeen kontuan hartuta, lau klasetan sailkatzen dira: (1) totipotenteak, ehun enbrionarioen zein ez-enbrionarioen (plazentaren) zelula guztietan bereizi daitezkeenak, eta organismo oso bat eratzeko gaitasuna dutenak; (2) pluripotenteak, leinu enbrionario guztietako zeluletan bereizi daitezkeenak; (3) multipotenteak, beren jatorriko leinu enbrionarioko zeluletan bakarrik bereizten direnak; eta (4) unipotenteak, zelula-mota bakar batean bereizten direnak. Gaitasun horri esker, zelula amek potentzial handia dute ehunak sendatzeko eta birsortzeko. Haien erabilera sakon aztertu da hezurren eta kartilagoaren berrikuntzan.
Birsortze-ahalmen horretaz gain, zelula amek beste efektu terapeutiko garrantzitsu bat dute: immunitate-sistema erregula dezakete. Haien ekintza immunomodulatzailea zenbait mekanismoren konbinazio konplexuaren emaitza bada ere, zelulek ekoizten eta askatzen dituzten faktore bioaktiboak jotzen dira jarduera horren arduradun nagusitzat. Haien artean, interleukinak, entzima metabolikoak, hazkuntza-faktoreak eta kimiokinak daude; zelula immuneekin elkarreragin eta haien efektua erregulatzen.
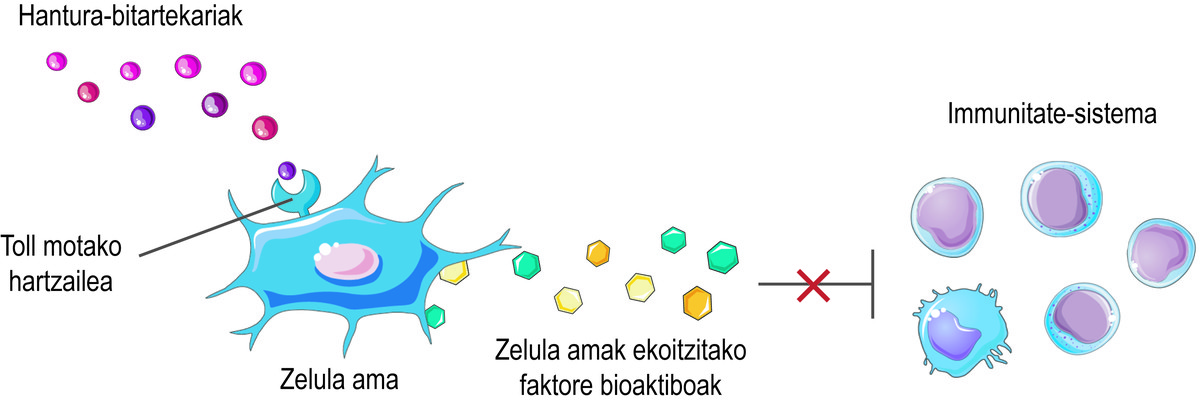
Baina, nola ote dakite zelula amek faktore bioaktiboak askatu behar dituztela? Zelula amek beren mikroingurunean gertatzen ari dena sumatzen dute, gainazalean dauzkaten Tollmotako hartzaileen bidez, eta egoera orekatzen saiatzen dira. Adibidez, lesio baten hasieran, hautematen dute ingurunean hantura-bitartekari gutxi daudela, eta immunitate-sistema aktibatzeko seinaletzat jotzen dute. Ondorioz, zelula amek erantzun immunea aktibatzen duten zenbait faktore bioaktibo jariatzen dituzte, lesio horren sendaketa-prozesuari hasiera emateko. Immunitate-sistemak bere funtzioa betetzen duen heinean, hantura-bitartekariak askatzen ditu. Horrela, prozesua burutzen denean, aipatutako hantura-bitartekarien maila altua da. Hori atzematean, zelula amek erantzun immunea inhibitzen duten faktore bioaktiboak askatzen dituzte, eta, hala, ehunen sendaketa eta homeostasia sustatzen dituzte (2. irudia).
Gaitz askotan immunitate-sistemaren gehiegizko aktibazioa gertatzen dela kontuan hartuz, zelula amak alternatiba terapeutiko bikaina bihurtu dira. Berez, erantzun immunea murriztuz, gaixotasunaren jatorrian eraso egiten dute. Besteak beste, zelula amen erabilera sakon aztertu da mentu versus ostalari gaixotasuna, hesteetako gaixotasun inflamatorioa edota esklerosi anizkoitza tratatzeko, eta emaitza itxaropentsuak lortu dira.
Zelula amen translazio klinikoa lortzeko gainditu behar ditugun erronkak
Etorkizun handiko terapia izan arren, zenbait erronka gainditu behar dira oraindik zelula ametan oinarritutako tratamenduak klinikara hurbiltzeko. Alde batetik, premiazkoa da emate-protokoloak optimizatzea. Zain barnetik eman ondoren, ostalariaren immunitate-sistemak ezabatu egiten ditu zelula amak denbora gutxian, eta nabarmen murrizten da terapiaren eraginkortasuna. Horretaz gain, zelulen portzentaje garrantzitsu bat biriketako kapilarretan pilatuta geratzen da, eta gainontzekoa gorputzean zabaltzen da. Horrek segurtasun-arazoak sor ditzake.
Bestalde, lehenago aipatu den moduan, hantura-bitartekarien presentzia ezinbestekoa da zelula amek immunitate-sistemaren eragina inhibitu dezaten. Arazoa da gaixotasun askotan bitartekari horien maila urria dela, eta, ondorioz, zelulek ez dute seinalerik jasotzen immunitatea mugatzen duten faktore bioaktiboak askatzeko. Hori dela eta, gaur egun, komunitate zientifikoa ahalegin handia egiten ari da zelula amen gaitasun immunomodulatzaileak sustatzen dituzten estrategiak garatzeko. Alternatiben artean, zelula amak hantura-bitartekariekin estimulatzea da nagusi, hots, hanturazko estimulazioa. Zehazki, frogatu da ezen eman aurretik, zelula amak gamma interferoiarekin (IFN-γ), alfa tumorearen nekrosi faktorearekin (TNF-α) edo antzeko beste hantura-bitartekari batzuekin estimulatzean, nabarmen hobetzen dela zenbait faktore bioaktiboren askapena. Alabaina, estimulazio honen eragina iragankorra da, eta egunen buruan desagertzen da. Zoritxarrez, hori ez da nahikoa gaixotasun kronikoak tratatzeko, eta, ondorioz, ezinbestekoa da zelula amen efektu erregulatzailea epe luzez mantentzen duten estrategiak aurkitzea.
Zelula amen ekintza terapeutikoa bultzatzen duten emate-sistemak
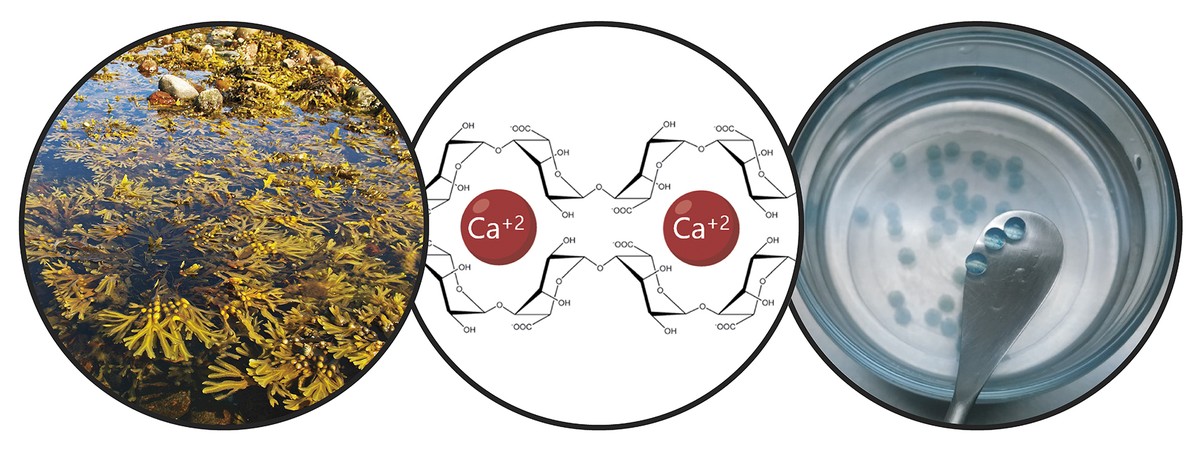
Aipatutako mugak kontuan hartuz, zelula amen erretentzioa eta ekintza terapeutikoa epe luzez bultzatzen dituen emate-sistema baten garatzea izan da tesiaren helburu nagusia. Zehazki, emate-sistema berri honetan, bi estrategia konbinatu ditugu. Alde batetik, zelulen erretentzioa bermatzeko eta haien bideragarritasuna sustatzeko, hidrogel batean kapsularatu ditugu. Hidrogel bat kate malguak dituen hiru dimentsioko sare-egitura bat da; gure kasuan, alginatoz eratua. Alginatoa alga marroietan aurkitzen den polimero natural bat da. Alginatoak eskaintzen dituen abantailen artean, hauek dira nabarmenenak: biobateragarritasuna, toxikotasun baxua eta kondizio arruntetan hidrogelak eratzeko gaitasuna. Ezaugarri horiek ezinbestekoak dira kapsularatze zelularraren teknologian. Alginato hidrogelakerretikulazio-metodobat baino gehiago erabiliz presta daitezke, baina erabiliena polimero-kateen eta katioi dibalenteen arteko gurutzaketa ionikoa da, zeina kaltzioaren bidez egiten baita maiz (3. irudia). Lortutako hidrogelek ur asko dute, eta baita ehun bigunekiko antzekotasun mekanikoak ere. Gure kasuan, alginatoak sortzen duen hiru dimentsioko sare horretan kolagenoa gehitu dugu, zelulen mikroingurune naturala imitatzean haien bideragarritasuna sustatzen baita.
Hidrogel horiek gorputzeko leku batean baino gehiagotan eman daitezke; esaterako, barrunbe peritonealean edo larruazalpean. Behin emanda, inplantea kokapen horretan geratuko da, eta zelulen erretentzioa bermatuko du. Bestalde, hidrogelak babestu egiten ditu zelula amak ostalariaren immunitate-sistematik, zelula immuneen eta antigorputzen sarrera saihesten baitu. Puntu honetan, garrantzitsua da zehaztea hidrogelaren egitura polimerikoak bide ematen duela zelula amek askatzen dituzten faktore bioaktiboak hedatzeko. Horrela, kapsulatutako zelulak emandako kokalekuan mantentzea eta faktore bioaktiboak era iraunkorrean askatzea ahalbidetzen du gure sistemak. Izan ere, saguekin egin ditugun saiakuntza aurreklinikoetan, zelula amak kapsulatzen dituzten hidrogelak larruazalpean mantendu dira epe luzez. Hain zuzen ere, jarri eta 45 egunera inplanteak berreskuratzean, zelulak aztertu ditugu, eta egiaztatu dugu bizirik jarraitzen dutela.
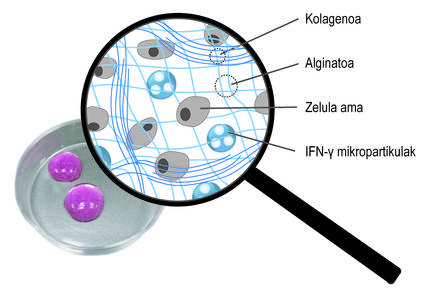
Hiru dimentsioko kapsulatzeaz gain, bigarren estrategia bat erabili dugu zelulen ekintza terapeutikoa sustatzeko. Zehazki, zelula amak hantura-bitartekariekin etengabe estimulatzea izan da ideia. Horretarako, IFN-γ bitartekariarekin kargatutako mikropartikula esferikoak gehitu ditugu alginato-kolageno hidrogelaren sare tridimentsionalean (4. irudia). Gure ikerketek frogatu dute sistema konbinatu horrek lortzen duela etengabeko hantura-mikroingurunea mantentzea. Hala, zelula amek denbora luzeagoan ekoizten dituzte immunitate-sistema inhibitzen duten faktore bioaktiboak. Bestalde, egiaztatu dugu ezen, hidrogel berri horietan kapsulatutako zelula amak immunitate-sistemaren zelulekin kultibatzean, azken horien efektua inhibitzen dela. Horrek agerian uzten du sistemak ondo funtzionatzen duela.
Orokorrean, bi estrategia horiek bateratzen dituen emate-sistema berri honek, zelulen ekintza terapeutikoa bultzatzeaz eta luzatzeaz gain, haien erretentzioa eta bideragarritasuna bermatzen ditu, eta horrek inplikazio garrantzitsuak izan ditzake zelula horietan oinarritutako terapietan.
Bibliografia
J. Galipeau and L. Sensebe, Cell. Stem Cell., 2018, 22, 824-833 (DOI:10.1016/j.stem.2018.05.004).
L. J. Scott, BioDrugs, 2018, 32, 627-634 (DOI:10.1007/s40259-018-0311-4).
K. Muroi, K. Miyamura, M. Okada, T. Yamashita, M. Murata, T. Ishikawa, N. Uike, M. Hidaka, R. Kobayashi, M. Imamura, J. Tanaka, K. Ohashi, S. Taniguchi, T. Ikeda, T. Eto, M. Mori, M. Yamaoka and K. Ozawa, Int. J. Hematol., 2016, 103, 243-250 (DOI:10.1007/s12185-015-1915-9).
A. Gonzalez-Pujana, K. H. Vining, D. K. Y. Zhang, E. Santos-Vizcaino, M. Igartua, R. M. Hernandez and D. J. Mooney, Biomaterials, 2020, 257, 120266 (DOI:S0142-9612(20)30512-3).
J. R. Ferreira, G. Q. Teixeira, S. G. Santos, M. A. Barbosa, G. Almeida-Porada and R. M. Goncalves, Front. Immunol., 2018, 9, 2837 (DOI:10.3389/fimmu.2018.02837).
A. Gonzalez-Pujana, M. Igartua, E. Santos-Vizcaino and R. M. Hernandez, Expert Opin. Drug Deliv., 2020, 17, 189-200 (DOI:10.1080/17425247.2020.1714587).

Gai honi buruzko eduki gehiago
Elhuyarrek garatutako teknologia



_galeria.jpg)