Las células también tienen oficinas de correo: coroideremia
2014/07/01 Mendizabal, Aitziber - Ondarroako BHI | Solozabal, Lourdes - Ondarroako BHI | Zarate, Jon - Farmazia Fakultatea, UPV/EHU | Elgezabal, Amaia - Koroideremiak Kaltetutakoen Elkartea | Olea, Fran - Koroideremiak Kaltetutakoen Elkartea Iturria: Elhuyar aldizkaria
Comenzamos en enero de 2014, tal y como prometimos al Olentzero, con el objetivo de que la Asociación de Afectados por la Coroideremia CHM, Proteína Rab Escort (REP1) Tipo 1, Rab27, RabGTPasa o Prenilación sea más conocida. La coroideremia es una enfermedad genética que sufre uno de cada 50.000 habitantes. En la región coroidal, el gen de la proteína Rep1, conocido como CHM, está afectado por una mutación. Por ello, los pacientes no sintetizan proteínas funcionales Rep1.
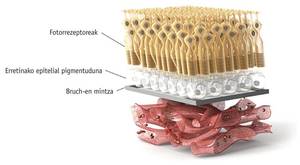
Dado que el gen CHM se encuentra en el cromosoma X sexual y tiene un carácter subyacente, la coroideremia es sufrida mayoritariamente por hombres, aunque también afecta a mujeres individuales. Los principales daños se observan en los ojos de los CHM mutados, en la propia retina y, como su propio nombre indica, en la coronación. Es evidente la degeneración de los tejidos de la retina que muestra la imagen profunda del ojo. En la zona coroidal, la coroides y la retina se inician alrededor del globo ocular y se degeneran hacia el fobear, creando la ceguera en la misma dirección, de fuera hacia dentro, siguiendo el patrón del efecto túnel. Al mismo tiempo, los pacientes pierden su sensibilidad a la luz y tienen problemas de visión cuando hay algo de oscuridad, lo que se conoce como ceguera nocturna.

La Rab Geranilgeranil transferasa (RGGTasa) es una enzima como cualquier otra enzima de naturaleza proteica, zona activa, etc. ¿Qué es, entonces, lo que le da tanta importancia como en este artículo?
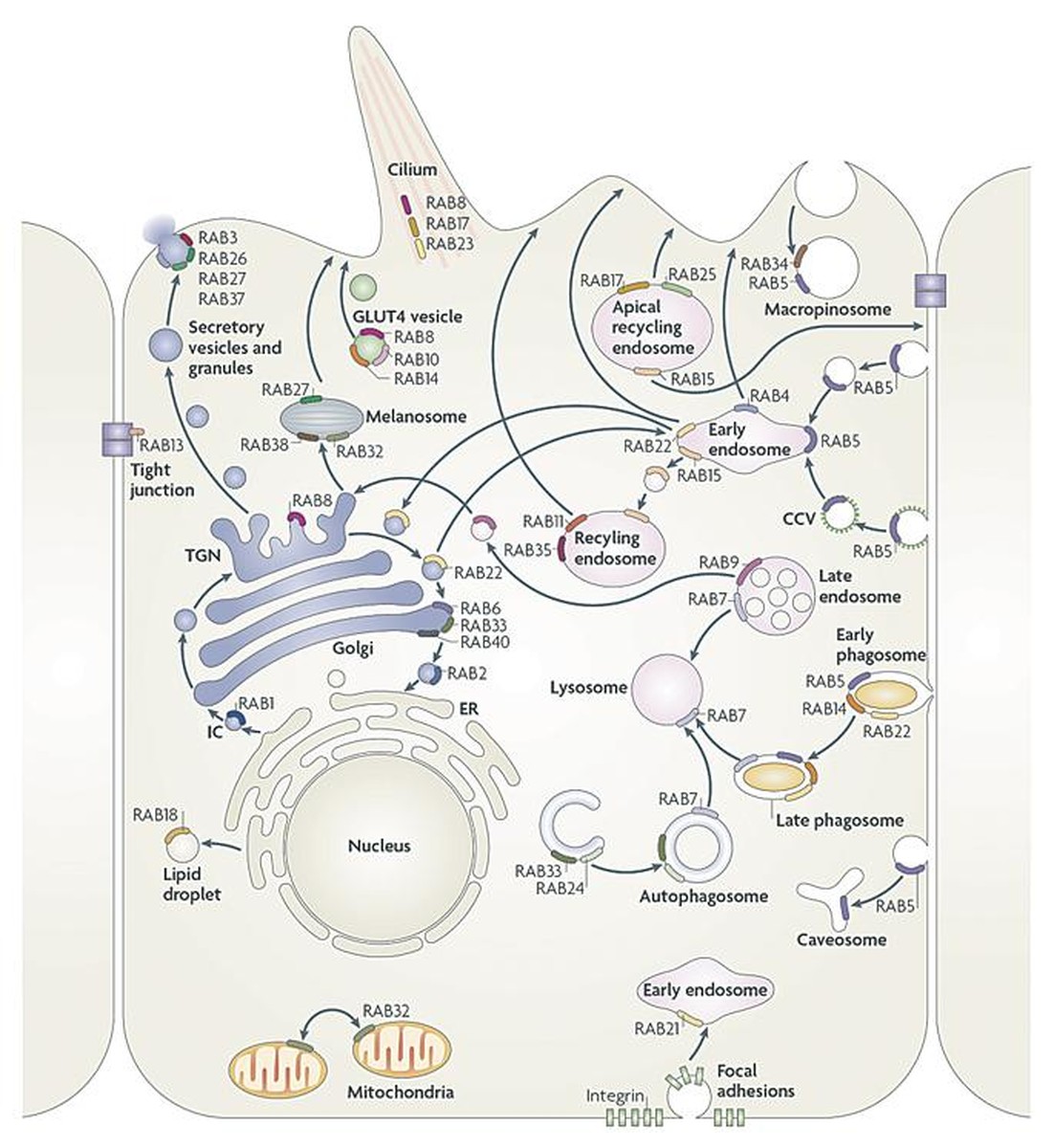
Si miramos hacia el interior de la célula vemos varias moléculas como si no llegara hasta aquí. Unos van unidos al citoesqueleto; otros, como si fueran cartas de correo, son transportados en jijones rodeados de membranas hasta que encuentran su camino. Este tipo de transporte por vesículas se realiza entre los diferentes compartimentos de la célula eucariota, como el aparato de Golgi, la red endoplasmática, los vacuolos, los melanocitos y la membrana externa.
¿Pero cómo saben a dónde tienen que ir? ¿Quién pone la dirección y el sello a los sobres? Pues para ello contamos con proteínas Rab (Rab GTPasas), pequeñas proteínas de una sola cadena polipeptídica. La dirección marcada por las proteínas rab depende del estado GTP(on)-GDP(off). Hay más de 60 rabs diferentes, cada uno se identifica por un número, y en el lenguaje de la célula cada uno indica una dirección diferente. Por ejemplo, Rab 27 marca melanocitos. Por tanto, cuando se forma una vesícula de transporte que se realiza entre los compartimentos de la célula, hay que asociar una proteína Rab para saber a dónde debe ser transportada. Al tratarse de una proteína hidrófoba, el rab se ancla a la parte hidrófoba de la membrana vesicular. Es aquí donde la enzima RGGTasa realiza su trabajo, pegando a los sobres la dirección correcta para que cada uno pueda ir a su sitio y realizar correctamente su función. Dicho de otro modo, la enzima RGGTasa es especialista en la prenilación de proteínas y prenilla a las RabGTPasas. Se llama prenilación o geranilgeranilación a la asociación del grupo geranil a las proteínas, es decir, a la cisteina aminoácido de la parte carboxilo terminal. Este isoprenoide de 20 carbono, RGGTasa, modifica la naturaleza de la proteína Rab, soluble en sí misma. Une dos colas hidrófobas a la proteína hidrófila Rab para que se ancle en el interior de la doble capa de la membrana.
La proteína chaperona Rep1(Rab escort protein 1) a RGGTasa ayudará a pegar la dirección correcta a los sobres. El txaperón Rep1 recogerá y moldeará la proteína Rab hasta que la enzima RGGTasa realice su trabajo y quede adherida a la proteína Rab. Contamos también con el txaperón Rep2, que realiza un trabajo similar al de Rep1, pero que por su menor afinidad con la enzima, no es capaz de hacer lo mismo que Rep1. Sin embargo, son necesarias las proteínas Rep, ya que si no las hay o si sufre daños en ellas, las proteínas Rab y las vesículas se acumulan en el citosol. En consecuencia, ciertas funciones que dependen de la exocitosis quedan sin desempeñar.
Como se ha mencionado anteriormente, las consecuencias de la falta de mecanismo de las proteínas Rep y Rab en la coroideremia son graves, por ejemplo, la ceguera. Sin embargo, para comprender mejor por qué se desarrolla la ceguera es necesario explicar mejor el mecanismo molecular. Rep1 es imprescindible para prenilar la proteína Rab27 en las células de la coroides. Debido a que en el citoplasma de las células oculares de pacientes con coroideremia el Rab27 no está prenilado, los melanocitos quedan sin marcadores. Esta carencia genera dos problemas principales. Por un lado, no se produce la exocitosis de los residuos necesarios para la función de mantenimiento de la coroides, y las células mueren debido a su alto grado de toxicidad. Por otro lado, dado que los melanocitos adecuadamente formados no pueden segregar melanina, la retina se queda sin protección óptica y se degenera. Las células fotoreceptoras de la retina requieren una renovación continua de la membrana de los discos mediante exocitosis. La renovación de la membrana es imprescindible para mantener funcionales las moléculas de rodopsina que convierten la quinada lumínica en un impulso nervioso. De hecho, la falta de funcionalidad de las moléculas de rodopsina es la causa principal del deslumbramiento de las personas coronadas.
Últimamente se han realizado algunos intentos de curación de la coroideremia. El pasado mes de enero se realizaron los primeros ensayos clínicos con terapia génica en el Reino Unido, en la Universidad de Oxford. El doctor Robert E McLaren transferió el gen CHM a 6 pacientes mediante terapia génica con virus. Si esta terapia para curar la retinopatía de la coroideremia resultase eficaz y segura, supondría una esperanza para otros pacientes que sufren la degeneración de la retina.
A pesar de nuestra gran esperanza en la terapia génica, no podemos descartar otras estrategias terapéuticas. En este sentido, merecen una mención especial los investigadores galardonados con el Premio Nobel de Medicina 2013. Los investigadores James Rotham, Randy Schekman y Thomas Südhof fueron premiados por sus investigaciones sobre transporte celular. Estos premios Nobel investigaron las proteínas Rep1 y RabGTPasa. La profundización en la investigación de estas proteínas incrementaría el conocimiento sobre el transporte y la secreción de enzimas, hormonas, neurotransmisores, etc. y abriría las puertas a nuevas estrategias terapéuticas para la zona coroidal. Hasta encontrar un medicamento que cure la coroideremia, deberíamos pensar también en la posibilidad de terapias que, en un plazo más breve, serían útiles para estos enfermos que se están quedando ciegos. Por ejemplo, se pueden investigar moléculas que han demostrado la capacidad de inertización de las células de la retina. Sin embargo, para demostrar la efectividad de todas estas estrategias que se proponen en este artículo, es necesario desarrollar modelos válidos para investigar la coroideremia y, si es posible, para evitar el uso de animales, que sean modelos in vitro. Asimismo, es necesario que el personal de investigación básica se incorpore a los clínicos y colabore en beneficio de los pacientes.
En lugar de ceder ante esta situación, en febrero de 2012 decidimos crear la Asociación de Afectados por la Coroideremia. Desde la creación de la Asociación, a nivel estatal, hemos contactado con 17 familias con coroideo y tenemos 61 socios. Además, los investigadores estamos constantemente luchando por recaudar fondos para poder desarrollar un tratamiento basado en la terapia génica antes de que nuestros hijos y asociados pierdan la vista. En este sentido, en colaboración con el IES de Ondarroa y el grupo de investigación NanoBioCel de la UPV/EHU, hemos organizado las primeras jornadas de investigación sobre la zona coroidal que tendrán lugar los días 16 y 17 de septiembre en la Facultad de Farmacia del Campus de Álava. En estas jornadas científicas se trabajará la coroideremia desde seis puntos de vista: clínica, fisiopatología y caracterización genético-molecular, terapia neuroprotectora, terapia génica, terapia celular, modelos in vitro e in vivo y ensayos clínicos.
Bibliografía

Gai honi buruzko eduki gehiago
Elhuyarrek garatutako teknologia